
【题目】过氧化钙可用于治理赤潮、应急供氧等。已知:过氧化钙,为白色或淡黄色结晶粉末,难溶于水,不溶于乙醇、乙醚等有机溶剂,常温下干燥品很稳定,能溶于稀酸生成过氧化氢。某小组同学探究过氧化钙的制法和性质:
(1)甲、乙两位同学设计的过氧化钙实验室制法如下,其中产率较低的是______(填A、B)
方法A Ca (OH)2 (s) + H2O2 CaO2 (s) + 2H2O
方法B CaCl2 (s) + H2O2 CaO2 (s) + 2HCl
方法A所得产品中纯度不高,所含杂质主要是 ___________(填化学式)
如果不加入稳定剂,则两种方法都需在5℃以下进行实验,原因可能是______________。
(2)丙同学认为CO2、SO2与过氧化钙的反应原理相同,丁同学认为SO2具有较强的还原性,而CO2没有,故而反应原理不相同。他们设计了如下实验装置,通过测量装置E中所得气体体积判断反应情况:
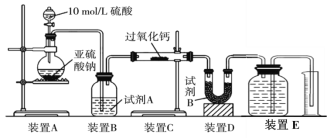
①试剂B的作用是____________________。
②若实验中SO2足量,且与过氧化钙充分反应,取反应后的固体进行探究,以验证过氧化钙与SO2反应的生成物。若SO2未被氧化,则反应的化学方程式为:______________________________。
③装置E中收集到的氧气体积为V L(已换算成标准状况下),若SO2完全被氧化,则V =______。
(3)某工厂利用电石渣(主要成分为氢氧化钙)生产过氧化钙的生产流程如下:
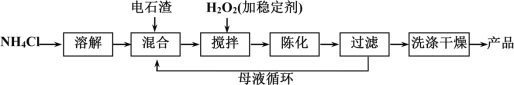
用上述方法制备过氧化钙(CaO2·8H2O),搅拌步骤的化学方程式是______________。
②某小组釆用单变量法确定温度、H2O2浓度对产率的影响,结果如下,则实际生产应选择的适宜条件为__________。
H2O2 % | 30% | 25% | 20% | 15% | 10% | 5% | ||||||
产率 | 60.40 | 62.42 | 64.54 | 63.20 | 63.10 | 62.40 | ||||||
温度(℃) | 50 | 40 | 30 | 20 | 10 | 0 | ||||||
产率 | 43.24 | 52.80 | 64.54 | 63.80 | 60.45 | 52.40 | ||||||
【答案】B Ca(OH)2 反应放热,使平衡向左移动,另外过氧化氢受热分解 吸收未反应的SO2 2CaO2+2SO2=2CaSO3+O2 0 CaCl2+H2O2+2NH3H2O+6H2O=CaO28H2O↓+2NH4Cl 温度为30℃、H2O2浓度为20%
【解析】
(1) 过氧化钙难溶于水,能溶于稀酸生成过氧化氢;根据反应物是否全部反应判断CaO2中含有的杂质,由于反应是放热反应,需要在较低温度下反应,另外H2O2不稳定,受热易分解;
(2)①SO2与CaO2反应生成的气体中可能混有未反应的SO2,需要利用试剂B除去;
②若SO2未被氧化,则SO2和过氧化钙反应生成亚硫酸钙和氧气;
③若SO2完全被氧化,则全部变为硫酸钙;
(3)主要成分为Ca(OH)2的电石渣与NH4Cl混合后得到CaCl2和NH3H2O,再加入H2O2和稳定剂,搅拌得到CaO28H2O,过滤、洗涤并干燥后得到产品;根据反应流程得出反应方程式,根据实际数据得出实际生产应选择的适宜条件。
(1)过氧化钙难溶于水,能溶于稀酸生成过氧化氢,因此甲、乙两位同学设计的过氧化钙实验室制法中方法B生成的CaO2要与HCl反应,导致产率低,故答案为B;方案A所得产品中纯度不高,主要是含有未反应的氢氧化钙;如果不加入稳定剂,则两种方法都需在5℃以下进行实验,原因可能是:①两个反应都是放热反应,为提高产率,促进平衡正向移动,则均需要在较低温度下进行,②避免H2O2在较高温度下分解;
(2)①反应生成的气体中可能混有未反应的SO2,需要利用试剂B除去,则试剂B的作用是吸收未反应的SO2;
②若SO2未被氧化,则二氧化硫和过氧化钙反应生成亚硫酸钙和氧气,发生反应的化学方程式为2CaO2+2SO2=2CaSO3+O2;
③若SO2完全被氧化,则全部变为硫酸钙,发生反应的化学方程式为CaO2+SO2=CaSO4,则没有氧气生成,即V=0;
(3)①根据反应流程可知,混合后得到CaCl2和NH3H2O的混合液,CaCl2和NH3H2O与H2O2混合搅拌生成CaO28H2O,则发生反应的化学方程式为CaCl2+H2O2+2NH3H2O+6H2O=CaO28H2O↓+2NH4Cl;
②根据表中数据可知温度为30℃、H2O2浓度为20%时CaO2·8H2O的产率最高,则实际生产应选择的适宜条件为温度为30℃、H2O2浓度为20%。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:______与盐酸反应最剧烈,____与盐酸反应的速度最慢;____与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为______________________________;
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_________,________________;
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律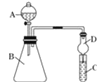
(4)干燥管D的作用为_______________;
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液________________________的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有______________溶液的洗气瓶.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
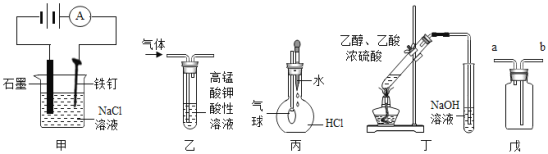
①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体
A.①⑤B.②④C.③④D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C—O | H—O | N—H | C—N | C—H |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 | 414 |
则该反应的ΔH=_________kJ·mol-1。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g) CH3OH(g) ΔH <0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
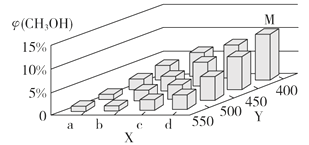
①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为_________。
②X轴上a点的数值比b点_________ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是________________________________。
(3)工业上可采用CH3OH CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通
CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通
过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为_________(填A、B)。
下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为______________________________________________。
(4)常温下,PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3 mol·L-1,则Ksp(PbI2)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是
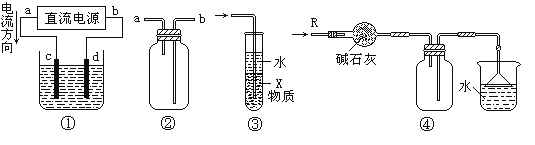
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式 ________________________。
(2)写出难溶电解质的溶度积表达式,Mg(OH)2:____________;在Mg(OH)2悬浊液中加入MgCl2固体,平衡________移动(填“正向”“逆向”或“不”),Ksp________(填“增大”“减小”或“不变”)。
(3)1 g固体炭与水蒸气反应生成CO气体和H2气体,需吸收a kJ热量,此反应的热化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置a、b、c中分别盛有试剂1、2、3,用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓 | Cu片 | KI-淀粉溶液 | 验证 |
|
B | 盐酸 | 石灰石 | 饱和 | 制备 | |
C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证溶液X中是否有 | |
D | 70%硫酸 |
| 酸性 | 证明 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是
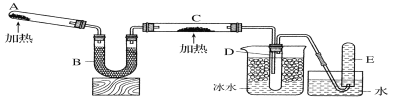
A.反应中氧化剂和还原剂的物质的量之比为2∶3
B.装置D中液体可以使干燥的红色石蕊试纸变蓝
C.装置B中加入的物质可以是碱石灰或无水氯化钙
D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s)![]() CaO(s) + CO2(g) △H1= +178.30kJ/mol
CaO(s) + CO2(g) △H1= +178.30kJ/mol
②CaO(s) + SO2(g) + 0.5O2(g)![]() CaSO4(s) △H2= -501.92 kJ/mol
CaSO4(s) △H2= -501.92 kJ/mol
③CO(g) + 0.5O2(g) ![]() CO2(g) △H3
CO2(g) △H3
④CaSO4(s) + CO(g) ![]() CaO(s) + SO2(g) + CO2(g) △H4= +218.92kJ/mol
CaO(s) + SO2(g) + CO2(g) △H4= +218.92kJ/mol
(1)温度升高,反应①的化学平衡常数________(填“增大”“减小”或“不变”)。
(2)△H3=________kJ/mol。
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com