
【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是 . a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 , 氧化性最弱的简单阳离子是(填离子符号) .
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
①工业制镁时,电解MgCl2而不电解MgO的原因是
②制铝时,电解Al2O3而不电解AlCl3的原因是; ③写出电解Al2O3反应方程式 .
【答案】
(1)b
(2)氩;Na+
(3)MgO的熔点高,熔融时消耗更多能量,增加生产成本;氯化铝是共价化合物,熔融态氯化铝难导电;2Al2O3(熔融) ![]() +4Al+3O2↑
+4Al+3O2↑
【解析】解:(1)a.第三周期中,随着原子序数的递增,原子半径逐渐减小,而离子半径需要根据阴阳离子进行讨论,阳离子只有2个电子层,随着核电荷数在增大,半径逐渐减小,而阴离子有3个电子层,随着核电荷数的增加逐渐减小,但是阴离子半径整体大于阳离子半径,从阳离子到阴离子,半径在增大,故a错误; b.同一周期中,随着核电荷数的递增,元素的金属性逐渐减弱,非金属性逐渐增强,故b正确;
c.元素的金属性越强,其最高价氧化物的水化物碱性越强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,所以其最高价氧化物的水化物碱性减弱、酸性增强,故c错误;
d.同一周期元素,其单质的熔点先增大后减小,Si的熔点最高,故d错误;
所以答案是:b;(2)原子最外层电子书与次外层电子数相同,而第三周期中次外层电子为8,该元素原子结构示意图为 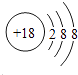 ,则该元素为氩;金属的还原性越强,对应离子的氧化性越弱,所以第三周期中氧化性最弱的为Na+ ,
,则该元素为氩;金属的还原性越强,对应离子的氧化性越弱,所以第三周期中氧化性最弱的为Na+ ,
所以答案是:氩;Na+;(3)①由于氧化镁的熔点远远大于氯化镁的熔点,熔融时消耗更多能量,增加生成成本,所以工业制镁时,采用电解MgCl2而不电解MgO,
所以答案是:MgO的熔点高,熔融时消耗更多能量,增加生产成本;
②由于氯化铝为共价化合物,熔融状态下氯化铝难导电,制锅时电解Al2O3而不电解AlCl3 ,
所以答案是:氯化铝是共价化合物,熔融态氯化铝难导电;
③电解氧化铝生成铝和氧气,电解时加入冰晶石以降低熔点,方程式为2Al2O3(熔融) ![]() +4Al+3O2↑,
+4Al+3O2↑,
所以答案是:2Al2O3(熔融) ![]() +4Al+3O2↑.
+4Al+3O2↑.


科目:高中化学 来源: 题型:
【题目】已知难溶性物质K2SO4MgSO42CaSO4在水中存在如下平衡:K2SO4MgSO42CaSO4 (s)2Ca2++2K++Mg2++4SO42﹣ . 不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是( ) 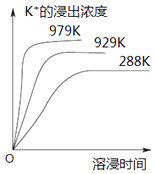
A.该平衡的Ksp=c2(Ca2+)c2(K+)c(Mg2+)c4(SO42﹣)
B.向该体系中加入饱和K2SO4溶液,溶解平衡向左移动
C.升高温度,溶浸速率增大,平衡向正反应方向移动
D.向该体系中加入饱和NaOH溶液,溶解平衡不发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M2O7x-与S2-在酸性溶液中发生如下反应:M2O7x-+3S2-+14H+2M3++3S↓+7H2O,则M2O7x-中M的化合价是( )
A. +2 B. +4 C. +6 D. +3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组采用分类思想、利用抽象方程式:A+H2O→B+C总结相关物质的知识。
(1)若A为单质:
①金属氧化物B常作为磁性材料,则元素A在周期表中的位置为_________。
②A是一种黄绿色气体单质,则生成物中弱电解质的结构式为_________。
③B能腐蚀玻璃,单质C为空气的主要成分之一,写出该反应的化学方程式: _________。
(2)若A为氧化物:
①A为淡黄色固体,则A的电子式为_________。
②A、C均能造成光化学烟雾,则生成1molB转移的电子数目为_________。
(3)若B俗称酒精,C是生活中食用醋的主要成分,则有机物A的名称是_________。另外,A为盐时还可能发生盐类的水解,用以总结水解的规律及微粒浓度的关系等知识。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A,标准状况下的密度为1.25g/L.B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,E有香味.它们之间的转化关系如图1所示: 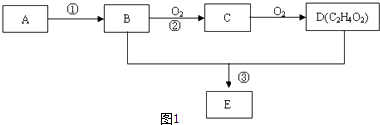
(1)A的电子式为 , D中官能团的名称为 .
(2)以A为原料自身合成高分子化合物的化学方程式为 , 反应类型是 .
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示).观察到的现象是 , 重复操作2﹣3次.写出过程②反应方程式 . 
(4)B、D在浓硫酸的作用下实现反应③,实验装置如图3所示: 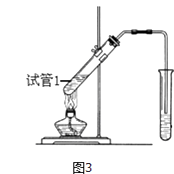
①试管1中实现反应③的化学方程式为 ,
②反应开始时用酒精灯对试管小火加热的原因是: . (已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经一定时间后,可逆反应aA+bBcC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( ) 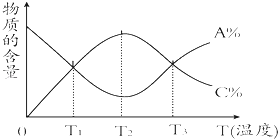
A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH相同的CH3COOH、HCl和H2SO4溶液,分别用蒸馏水稀释到原来的X、Y、Z倍,稀释后三种溶液的pH仍然相同,则X、Y、Z的关系是( )
A.X=Y=Z
B.X=Y<Z
C.X>Y=Z
D.X<Y=Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质发生的变化中,所克服的粒子间的作用(力)属同种类型的是( )
A.酒精和食盐溶于水
B.石英(SiO2)和生石灰的熔化
C.氯化钠固体和冰的融化
D.碘和干冰的升华
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com