

- 2 |
- 3 |
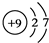 ,
,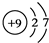 ;
; ,
, ;
;

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| B、放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 |
| C、化学反应中能量变化,通常主要表现为热量的变化------放热或者吸热 |
| D、凡经加热而发生的化学反应都是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B、若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C、若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D、若M属于离子化合物,则该化合物中只存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | 样品质量 | 消耗高锰酸钾 | 测定值 | 纯度 |
| g | mL | g | % | |
| 1 | 0.0514 | 5.46 | 0.0309 | 60.04 |
| 2 | 0.0479 | 5.11 | 0.0289 | 60.30 |
| 3 | 0.0522 | 6.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com