
【题目】I.一定温度下将6mol的A及6molB混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36mol/(L·min)。求:
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36mol/(L·min)。求:
(1)平衡时D的浓度= ,
(2)B的平均反应速率v(B)= ,
(3)x= ,
(4)开始时容器中的压强与平衡时的压强之比为 (化为最箭整数比)
II.将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)

(5) (填A或B)处电极入口通甲烷,其电极反应式为 ;
(6)当消耗甲烷的体积为11.2 L(标准状况下)时,则消耗KOH的物质的量为 。
(7)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2mol·L-1的KOH溶液,电池总反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为 ;每消耗3.4gNH3转移的电子数目为 。
【答案】
I.(1)1.2mol/L;(2)0.12mol/(Lmin);(3)3;(4)10:11;
II.(5)B;CH4 -8e- +10OH-═CO32- +7H2O;(6)1mol;(7)2NH3+6OH- -6e- =N2 +6H2O;0.6NA。
【解析】
试题分析:3A(g)+B(g)![]() xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转
化率为60%,则 3A(g)+B(g)![]() xC(g)+2D(g),
xC(g)+2D(g),
开始(mol/L) 3 3 0 0
转化(mol/L)3×60% 0.6 0.6x 1.2
平衡(mol/L) 1.2 2.4 0.6x 1.2
(1)由上述分析可知平衡状态D的浓度为1.2mol/L;(2)B的平均反应速率υ(B)=0.6mol/L ÷ 5min =0.12mol/(Lmin);(3)由速率之比等于化学计量数之比可知,1/x=0.12/0.36,解得x=3;(4)开始时容器中的压强与平衡时的压强之比等于反应前后的物质的量之和的比,为(6+6)mol:(1.2+2.4+0.6×3+1.2)mol/L×2L=10:11;II.(5)根据电子流向知,B为负极、A为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,所以B处通入甲烷,甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH4 -8e- +10OH-═CO32- +7H2O;(6)甲烷的物质的量为n(CH4)= 11.2L÷22.4L/mol=0.5mol,根据CH4 -8e- +10OH-═CO32- +7H2O可知反应消耗KOH的物质的量为甲烷物质的量的10倍,所以消耗氢氧化钾的物质的量是1mol;(7)电池反应为:4NH3+3O2=2N2+6H2O,该电池负极是氨气失电子生成氮气,反应的电极反应式为2NH3+6OH- -6e- =N2 +6H2O,反应中2mol氨气反应电子转移6mol电子,每消耗3.4g NH3物质的量n(NH3)=3.4g÷17g/mol=0.2mol,转移的电子数为0.6NA。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为 ;已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是 。
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,分子构型分别为 ,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se Si(填“>”、“<”)。
(3)SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为 ;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为 。
(4)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为 ,B与N之间形成 键。
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为 ,在SiC中,每个C原子周围最近的C原子数目为 个;若晶胞的边长为a pm,则金刚砂的密度表达式为 g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水淡化及海水资源的提取利用是当今化工行业重要课题。
回答下列问题:
(1)下列属于海水淡化常见工艺的是________(填序号)。
①电渗析法 ②蒸馏法 ③离子交换法 ④沉淀法
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是 Br2+Na2CO3+H2O→ NaBr+NaBrO3+NaHCO3,吸收1 mol Br2时,转移的电子为________mol。
(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:

该工艺过程中,脱硫阶段主要反应的离子方程式为____________________________________________,产品2 的化学式为________,1 L 浓海水最多可得到产品2 的质量为________g。
(4)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为:_______________。电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:___________。
(2)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银.
①(H3PO2)中,磷元素的化合价为___________。
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为:___________(填化学式);
③NaH2PO2是 正盐还是酸式盐?___________,其溶液显___________性(填“弱酸性”、“中性”、或者“弱碱性”)。
(3)H3PO2的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成PH3气体和Ba(H2PO2)2,后者再与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式___________。
(4)(H3PO2)也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式___________;
②分析产品室可得到H3PO2的原因___________;
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室,其缺点是___________杂质。该杂质产生的原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃,其球棍模型下图:

(1)等质量的以上物质完全燃烧时耗去O2的量最多的是___________(填对应字母,下同);
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是___________;
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是__________________;
(4)在120℃、1.01×l05Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N和Si是合成新型非金属材料的两种重要元素。请回答:
(1)基态Si原子的价层电子排布图为 ;Si原子可形成多种氢化物,其中Si2H6中Si原子的价层电子对数目为 。
(2)ClO3-、ClO4-中Cl都是以 轨道与O原子 轨道成键,其微粒的立体结构分别为 、 。
(3)N和Si形成的原子晶体中,N原子的配位数为 。
(4)NaN3常作为汽车安全气囊的填充物,其焰色反应为黄色。大多数金属元素有焰色反应的微观原因为 ;N3-中σ键和π键的数目之比为 。B、F与N三种元素同周期,三种基态原子的第一电离能由大到小的顺序为 (用元素符号表示)
(5)SiO2的晶胞与金刚石(如图所示)相似,可以看作Si原子替代C原子后,在两个成键的Si原子间插入1个O原子形成。则:
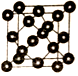
①晶胞中最小的环含有_____个原子。
②若晶体密度为ρg·cm3,阿伏伽德罗常数为NA,晶胞中两个最近的Si原子核之间的距离为____pm(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿原酸是金银花的主要抗菌、抗病毒有效药理成分之一。
Ⅰ.已知绿原酸X的结构简式为
(1)X中含氧原子的官能团的名称为____ _。
(2)下列叙述正确的是 _。
①X的分子式为C16O20O9
②1molX最多能与4mol H2发生加成反应
③X能与碳酸氢钠溶液反应,且能使酸性高锰酸钾褪色
④1molX最多能与5mol NaOH反应
⑤绿原酸水解后所得两产物碳原子数之差为2
Ⅱ.绿原酸在一定条件下可合成D和对羟基苯甲酸两种医药中间体,其合成路线如下(部分反应条件未注明):

已知:R—![]() —R
—R![]() 2R—CHO
2R—CHO
(1) D是一种芳香族化合物,D的结构简式为 ;
(2)A→C的反应类型是 ;
(3)由B生成E的化学方程式为 ;
(4)F与E互为同分异构体,且F同时满足下列条件:
①遇氯化铁溶液显紫色
②能发生银镜反应
③核磁共振氢谱为4组峰,且面积比为2:2:1:1,则F的结构共有 种(不考虑立体异构),结构简式为 (任写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3的化工厂利用钡泥制取Ba(NO3)2晶体及其他副产物,其部分工艺流程如下:
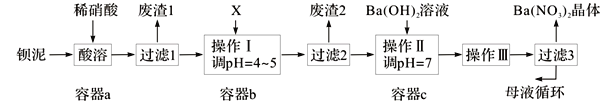
已知:i .Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7。
ii .Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小。
iii. Kap(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。
(1)Ba(FeO2)2中Fe的化合价是 。
(2)二氧化碳与水作用形成的碳酸在水中的电离常数Ka1=4.2×10-7 ,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 。
(3)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式和必要的文字说明提纯原理: 。
(4)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为: 。
(5)该厂结合本厂实际,选用的X为 (从下列选项中选择);废渣2为 (写出化学式)。
① BaCl2 ②Ba(NO3)2 ③BaCO3 ④ Ba(OH)2
(6)过滤3后的母液应循环到容器 中。(填“a”、“b”或“c”)
(7)称取w g晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m g,则该Ba(NO3)2的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下中的实验装置可用于制取乙炔。 请填空:
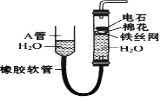
(1) 图中,A管的作用是_______________;制取乙炔的化学方程式是 。
(2)乙炔通入溴的CCl4溶液中观察到的现象是____________ ;乙炔发生了________反应。
(3)写出由乙炔制取聚氯乙烯的化学方程 、 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com