
科目:高中化学 来源:不详 题型:问答题
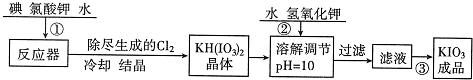
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3/100gH2O | 8.08 | 12.6 | 18.3 | 24.8 |
| 实验步骤 | 实验操作 | 实验现象 |
| 步骤1 | 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 步骤2 | 滴入5滴淀粉溶液和1mL0.1 mol?L-1KI溶液,振荡. | 溶液无变化 |
| 步骤3 | 然后再滴入1滴1 mol?L-1的H2SO4,振荡. | 溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu(Fe)----加稀硫酸,蒸馏 |
| B.CO2(SO2)----氢氧化钠溶液,洗气 |
| C.NaCl溶液(碘)----酒精,萃取、分液 |
| D.KNO3溶液(KCl)----降温结晶,过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
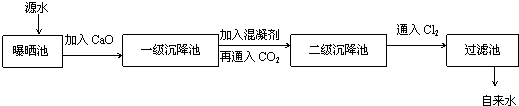
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 编号 | 物质 | 试剂名称或化学式 |
| ① | 除杂质:NaHCO3溶液(Na2CO3) | ______ |
| ② | 除杂质:SiO2(CaCO3) | ______ |
| ③ | 除杂质:FeCl2溶液(FeCl3) | ______ |
| ④ | 鉴别:Na2CO3Na2SiO3Na2SO3溶液 | ______ |
| ⑤ | 鉴别:(NH4)2SO4NH4Cl Na2SO4溶液 | ______ |
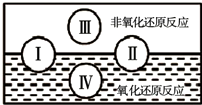
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 滴入稀HNO3同时用pH计测定至溶液呈中性 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| ③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
| A.①②③ | B.②③④ | C.①③④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入BaCl2溶液,生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含有SO42- |
| B.向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中滴几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
| C.用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含有K+ |
| D.加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com