
【题目】[化学——选修 3:物质结构与性质]
(1) 过渡金属元素铁能形成多种配合物,如:[Fe (CN) 6] 4-、[Fe(SCN)6]3-等。
Fe3+的核外电子排布式为______________,从原子结构的角度解释Fe3+比Fe2+稳定的理由是_______________。
(2) N的基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3) (NH4)2SO4阴离子的立体构型是________,NH4+中心原子的杂化类型是________。
(4) Fe有δ、γ、α三种同素异形体,其晶胞结构如下图所示:
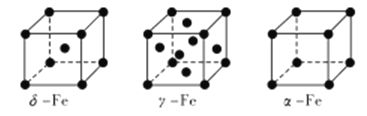
① δ、α两种晶体晶胞中铁原子的配位数之比为_____________。
②1个γ晶体晶胞中所含有的铁原子数为_____________。
③若Fe原子半径为rpm,NA表示阿伏加德罗常数的值,则δ-Fe单质的密度为____________g/cm3(列出算式即可)。
【答案】 [Ar]3d5 Fe3+的3d轨道为半充满状态,能量低稳定 3 哑铃(或纺锤) 正四面体形 sp3 4:3 4 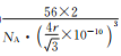
【解析】(1)Fe为26号元素,Fe3+的核外电子排布式为[Ar]3d5,Fe3+的3d轨道为半充满状态,能量低稳定,故Fe3+比Fe2+稳定;(2)因为氮原子的最外层有5个电子,其中2个是成对的,剩下的三个电子占据了三个p轨道,并且垂直分布,这样能量才能最低,则N的基态原子电子云在空间有3个方向,原子轨道呈哑铃或纺锤形;(3)(NH4)2SO4阴离子SO42-的中心S原子的价层电子对为:孤对电子数6-2×4+2=0,成键电子对数4,sp3杂化,其立体构型是四面体形;NH4+中N原子杂化轨道数为![]() ×(5+4-1)=4,采取sp3杂化方式;(4)①根据晶胞的结构可知,δ晶胞中以顶点铁原子为例,与之距离最近的铁原子是体心上的铁原子,这样的原子有8个,所以铁原子的配位数为8,α晶胞中以顶点铁原子为例,与之距离最近的铁原子是与之相连的顶点上的铁原子,这样的原子有6个,所以铁原子的配位数为6,所以δ、α两种晶体晶胞中铁原子的配位数之比为4:3;②利用均摊法计算得γ晶体晶胞中所含有的铁原子数为8×
×(5+4-1)=4,采取sp3杂化方式;(4)①根据晶胞的结构可知,δ晶胞中以顶点铁原子为例,与之距离最近的铁原子是体心上的铁原子,这样的原子有8个,所以铁原子的配位数为8,α晶胞中以顶点铁原子为例,与之距离最近的铁原子是与之相连的顶点上的铁原子,这样的原子有6个,所以铁原子的配位数为6,所以δ、α两种晶体晶胞中铁原子的配位数之比为4:3;②利用均摊法计算得γ晶体晶胞中所含有的铁原子数为8×![]() +6×
+6×![]() =4;③由晶胞示意图可知,δ-Fe单质为体心立方堆积,铁原子为面心和顶点,则一个晶胞中Fe的个数为1+8×
=4;③由晶胞示意图可知,δ-Fe单质为体心立方堆积,铁原子为面心和顶点,则一个晶胞中Fe的个数为1+8×![]() =2,一个晶胞的质量为
=2,一个晶胞的质量为![]() ,体心结构中,体对角线长为4rpm,晶胞边长为
,体心结构中,体对角线长为4rpm,晶胞边长为![]() ,晶胞体积为
,晶胞体积为![]() cm3,故密度为
cm3,故密度为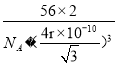 。
。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.HCl属于共价化合物,溶于水能电离出H+和Clˉ
B.NaOH是离子化合物,该物质中只含有离子键
C.HI气体受热分解的过程中,只需克服分子间作用力
D.石英和干冰均由原子构成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离常数(Ka或Kb)、溶度积常数(Ksp)是判断物质性质的重要常数,下列关于这些常数的计算或运用正确的是( )
A. 某亚硫酸溶液pH=4.3,若忽略二级电离,则其一级电离平衡常数K1=1.0×10-8.60
B. Ka(HCN)<Ka(CH3COOH),说明同浓度时氢氰酸的酸性比醋酸强
C. Ksp(AgI)<Ksp(AgCl),向AgCl悬浊液中加入KI溶液会出现黄色沉淀
D. Ksp(AgCl)<Ksp(AgOH),说明AgOH和AgCl均不溶于稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+3B(g) ![]() 2c(g)+D(g)在四种不同条件下的反应速率分别为( )。
2c(g)+D(g)在四种不同条件下的反应速率分别为( )。
①v(A)=0.5 mol/(L·min) ②v(B)=0.6 mol/(L·min)
③v(C)=0.35 mol/(L·min) ④v(D)=0.4 mol/(L·min)
则该反应在不同条件下反应速率最快的是( )
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等.利用炼铝厂的废料﹣铝灰(含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾.工艺流程如下:
回答下列问题:

(1)明矾净水的原理是(用离子方程表示)________________;
(2)操作Ⅰ是________,操作Ⅱ是蒸发浓缩、________、过滤、洗涤、干燥.
(3)检验滤液A中是否存在Fe2+的试剂是________(只用一种试剂)
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下Fe2+ 转化为Fe3+,MnO4﹣转化为Mn2+)________________。
已知:生成氢氧化物沉淀的pH如下表所示
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1mol·L﹣1
根据表中数据解释调pH=3的目的________________。
(5)已知:在pH=3、加热条件下,MnO4﹣可与Mn2+反应生成MnO2.加入MnSO4发生反应的离子方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图所示为锌铜原电池。下列叙述中,正确的是
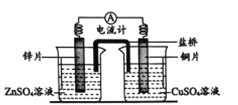
A. 盐桥的作用是传导离子
B. 外电路电子由铜片流向锌片
C. 锌片上的电极反应式为Zn2+ +2e- = Zn
D. 外电路中有0.2 mol 电子通过时,铜片表面增重约3.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 常温下,向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大
B. 0.1 mol·L-1的醋酸加水稀释,c(CH3COOH)/c(CH3COO-)减小,但K不变。
C. 足量体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少
D. 25℃,在AgCl悬浊液中加入少量NaCl固体,c(Ag+)减小,Ksp(AgCl)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(Ⅰ)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g。
请完成以下实验设计表,并在实验目的一栏中填空:
实验 编号 | 温度 (℃) | 大理石 规格 | HNO3浓度(mol/L) | 实验目的 |
① | 25 | 粗颗粒 | 2.00 | (I)实验①和②探究浓度对反应速率的影响; (II)实验①和③探究温度对反应速率的影响; (III)实验①和④探究______________对反应速率的影响 |
② | 25 | 粗颗粒 | _______ | |
③ | _____ | 粗颗粒 | 2.00 | |
④ | 25 | 细颗粒 | 2.00 |
(Ⅱ)把2.5 mol A和2.5 mol B混合放入2 L密闭容器里,发生反应:3A(g)+B(g)![]() xC(g)+2D(g),经5 s后反应达平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
xC(g)+2D(g),经5 s后反应达平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
(1)达平衡时B的转化率为_____________________。
(2)x的值为___________________。
(3)若温度不变,达平衡时容器内气体的压强是反应前的____________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
Ⅰ.已知:①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH=+93.0kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③CH3OH(g)=CH3OH(l) ΔH=-38.19 kJ·mol-1
则表示CH3OH的燃烧热的热化学方程式为______________________________________________。
Ⅱ.在一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g),在2L恒容密闭容器中充入1mol CO和2molH2,在催化剂作用下充分反应。下图表示平衡混合物中CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
CH3OH(g),在2L恒容密闭容器中充入1mol CO和2molH2,在催化剂作用下充分反应。下图表示平衡混合物中CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
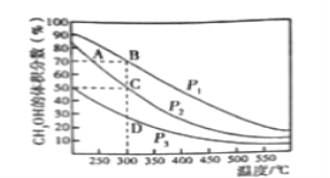
(1)该反应的反应热ΔH_______0(填“>”或“<”),压强的相对大小:p1_______p2(填“>”或“<”)。
(2)压强为p2,温度为300℃时,该反应的化学平衡常数K=________________。
(3)下列各项中,不能说明该反应已经达到平衡的是________________________________。
A.容器内气体压强不再变化 B.v(CO):c(H2):v(CO3OH)=1:2:1
C.容器内的密度不在变化 D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
(4)某温度下在保证H2浓度不变的情况下,增大容器的体积,平衡_________(填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
作出此判断的依据是__________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com