
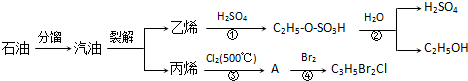
| △ |
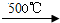 CH2ClCH=CH2+HCl,故答案为:CH3CH=CH2+Cl2
CH2ClCH=CH2+HCl,故答案为:CH3CH=CH2+Cl2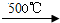 CH2ClCH=CH2+HCl;
CH2ClCH=CH2+HCl;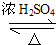 CH2(OOCCH3)CH(OOCCH3)CH2OOCCH3+3H2O,
CH2(OOCCH3)CH(OOCCH3)CH2OOCCH3+3H2O,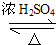 CH2(OOCCH3)CH(OOCCH3)CH2OOCCH3+3H2O.
CH2(OOCCH3)CH(OOCCH3)CH2OOCCH3+3H2O.


科目:高中化学 来源: 题型:
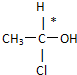 等,下列化合物中存在对映异构体的是( )
等,下列化合物中存在对映异构体的是( )| A、C2H5CH═CHCH(CH3)CH═CHC2H5 |
B、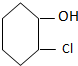 |
| C、甲酸 |
| D、C6H5COCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
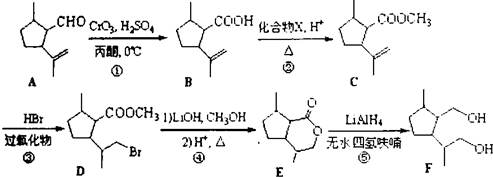
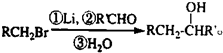 化合物
化合物  是合成抗癌药物白黎芦醇的中间体,请写出以
是合成抗癌药物白黎芦醇的中间体,请写出以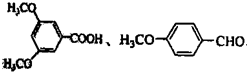 和CH3OH为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2
和CH3OH为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向稀盐酸中加入少量钠粒:2Na+2H2O=2Na++2OH-+H2↑ |
| B、向氯化铁溶液中滴加偏铝酸钠溶液:Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓ |
| C、Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++HCO3-+OH-=MgCO3↓+H2O |
| D、向含氯化铝的氯化镁溶液中加入氧化镁:Al3++MgO+H2O=Al(OH)3↓+Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
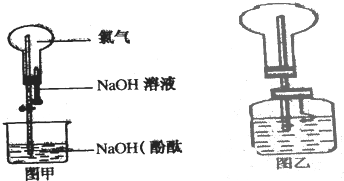 某研究性学习小组在做Cl2的喷泉实验时(图甲),发现含有酚酞的NaOHaq喷入烧瓶后,溶液的红色褪去,甲、乙两同学对此现象分别做了如下推测:
某研究性学习小组在做Cl2的喷泉实验时(图甲),发现含有酚酞的NaOHaq喷入烧瓶后,溶液的红色褪去,甲、乙两同学对此现象分别做了如下推测:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温下,0.1mol/L CH3COONH4溶液和0.1mol/L CH3C00Na溶液中,由水电离的c(H+),前者小于后者 |
| B、反应2A(s)+B(g)═2C(g)+D(g)不能自发进行,则该反应△H一定大于0 |
| C、同温下,已知醋酸电离平衡常熟为Ka,醋酸根水解常数为Kb,水的离子积为Kw.则三者关系为:Ka?Kb=Kw |
| D、反应A(g)?2B(g)△H,若正反应的活化能为EakJ?mol-1,逆反应的活化能为EbkJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
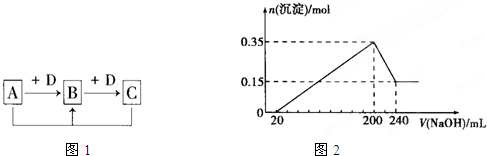
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
| B、1 L 0.1 mol?L-1 CuSO4?(NH4)2SO4?6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| C、0.1 mol?L-1 NaHSO3溶液中:c(H+)+c(H2SO3)=c(SO32-)+c(OH-) |
| D、等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com