
下列说法正确的是
A. 凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物
B. 两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体
C. 两种物质如果互为同分异构体,则它们的命名可能一样
D. 组成元素的质量分数相同,且相对分子质量也相同的不同化合物,一定互为同分异构体
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源:2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷(解析版) 题型:填空题
根据要求完成下列问题:
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:
该元素价电子排布式_____________________。
(2)外围电子排布式为3d54s2的原子,其原子结构示意图为____________,其最高正价为________;其在元素周期表中的位置为:___________________。
(3)下列分子中是否有手性原子:_________(填“有”或“无”,若有请在图中碳原子下方用“*”标出)
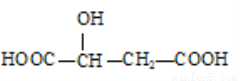
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧、PCl3中,属于非极性分子的是(填番号)________________。
(5) 试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):
HClO3________HClO4; H3PO4________H3PO3。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高一上学期期末检测化学试卷(解析版) 题型:选择题
下列气体中,既可用浓硫酸干燥,又可用固体NaOH干燥的是
A. Cl2 B. O2 C. SO2 D. NH3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二3月学生学业能力调研化学试卷(解析版) 题型:选择题
对于苯乙烯(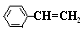 )的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯;⑤能发生硝化反应;⑥所有的原子可能共平面。其中正确的是
)的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯;⑤能发生硝化反应;⑥所有的原子可能共平面。其中正确的是
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二3月学生学业能力调研化学试卷(解析版) 题型:选择题
下列关于同分异构体判断正确的是( )
A. 分子式为C8H10的芳香烃有3个,分别为 、
、 和
和
B. 分子式为C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3
C. 甲烷是正四面体结构,则 和
和  不是同一个物质
不是同一个物质
D. 分子式为C2H6O的同分异构体有两个,分别是CH3OCH3和CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2017届浙江省绍兴市高三3月教学质量调测考试化学试卷(解析版) 题型:简答题
研究含氮和含硫化合物的性质在工业生产和环境保护中有重要意义。
(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)=2SO3(g) △H=-198kJ·mol-1
SO2(g)+NO2(g)=SO3(g)+NO(g) △H=-41.8kJ·mol-1
若CO的燃烧热为283 kJ·mol-1,则1molNO2和1mol CO 反应生成CO2和NO的能量变化示意图中E2= _________kJ·mol-1

(2)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g) S(I)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:_________
S(I)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:_________
②第8分钟时,保持其他条件不变,将容器体积迅速压缩至1L,在10分钟时达到平衡,CO的物质的量变化了1mol。请在图B中画出SO2浓度从6~11分钟的变化曲线。

(3)己知某温度下,H2SO3的电离常数为K1≈l.5×10-2, K2≈1.0×10-7,用NaOH溶液吸收SO2,当溶液中HSO3-, SO32-离子相等时,溶液的pH值约为_________
(4)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为_________,连二亚硫酸根与HNO2反应的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省绍兴市高三3月教学质量调测考试化学试卷(解析版) 题型:选择题
常温下,向l L pH=l0的NaOH溶液中持续通入CO2。通入CO2的体积(y)与溶液中水电离出的c(OH-)的关系如图所示。下列叙述错误的是
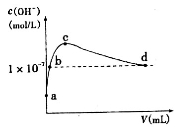
A.a点溶液中:水电离出的c(H+)=1×10-10mol·L-1
B.b点溶液中:c(H+)=1×10-7mol·L-1
C.c点溶液中:c(Na+)>c(HCO3-)>c(CO32-)
D.d点溶液中:c(Na+)=2c(CO32-)+c(HCO3-)
查看答案和解析>>
科目:高中化学 来源:2017届浙江省绍兴市高三3月教学质量调测考试化学试卷(解析版) 题型:选择题
关于金属钠单质及其化合物的说法中,不正确的是( )
A. NaCl可用作食品调味剂 B. 相同温度下NaHCO3溶解度大子Na2CO3
C. Na2CO3的焰色反应呈黄色 D. 工业上Na可用于制备钛、锆等金属
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二3月月考化学试卷(解析版) 题型:填空题
软锰矿的主要成分为MnO2,含少量Al2O3和SiO2。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下(中间产物的固体部分已经略去)。

已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式______。
(2)步骤③中MnO2的其作用是______,另外一种物质X可以是______。
A.MgCO3 B.ZnO C.MnCO3 D.Cu(OH)2
(3)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式______。MnO2可做超级电容器材料,用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是______.
(4)已知:H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______。[已知:Ksp(MnS)=1.4×10―15]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com