
| ����̿��mol�� | NO��mol�� | CO2��mol�� | N2��mol�� | |
| ��ʼ״̬ | 3.0 | 0.8 | 0 | 0 |
| 2minʱ | 2.8 | 0.4 | 0.2 | 0.2 |
���� ��1����Ӧ����ƽ��״̬ʱ�����淴Ӧ������ȣ�ͬ�����ʣ������淴Ӧ����֮�ȵ���ϵ��֮�ȣ���ͬ���ʣ���ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯�����ɴ˽����жϣ�
��2������v=$\frac{��c}{��t}$��������⣻
��3����֪�����¶ȣ��ÿ��淴Ӧ�Ļ�ѧƽ�ⳣ��K����˵��ƽ�������ƶ�����������Ӧ�����ȷ�Ӧ���Ƚ�Ũ���̺�ƽ�ⳣ���Ĵ�С��ϵ��NO��ƽ��ת����Ϊ$\frac{�仯��}{��ʼ��}��100%$��
��4��a����ѹʱ���������г��뺤�����������Ũ�ȱ�С�����Է�Ӧ���ʼ�С��
b������Ӧ�����ȷ�Ӧ�������¶ȣ���ѧƽ�������ƶ���
c������NO��Ũ�ȣ��൱������ѹǿ��ƽ�ⲻ�ƶ�������NO��ת���ʲ��䣻
d��ƽ�ⳣ�����¶ȵĺ�����
��� �⣺��1��a����λʱ��������2mol NO��Ч������1mol N2��ͬʱ����1mol N2�����淴Ӧ������ȣ���ƽ��״̬������ȷ��
b��NO���ʵ�����CO2���ʵ���֮��Ϊ2��1�������Dz��䣬�ʴ���
c�������������У����������л�������ѹǿʼ�ղ��䣬�ʴ���
d�����������ܶȲ��䣬˵��������������䣬���淴Ӧ������ȣ�����ȷ����ѡ��a��d��
��2��v=$\frac{��c}{��t}$=$\frac{\frac{0.8-0.4}{2}}{2}$=0.1mol?L-1?min-1���ʴ�Ϊ��0.1��
��3����֪�����¶ȣ��ÿ��淴Ӧ�Ļ�ѧƽ�ⳣ��K����˵��ƽ�������ƶ�����������Ӧ�����ȷ�Ӧ��Qc=$\frac{\frac{0.2}{2}��\frac{0.2}{2}}{��\frac{0.4}{2}��^{2}}$=0.25��K=9/16������ƽ�������ƶ���������Ӧ���ʴ����淴Ӧ���ʣ�
C��s��+2NO��g��?CO2��g��+N2��g����
��ʼ����3 0.8 0 0
�仯����x 2x x x
ƽ������0.8-2x x x
����K=$\frac{��\frac{x}{2}��^{2}}{��\frac{0.8-x}{2}��^{2}}=\frac{9}{16}$����֮��x=0.12mol��
NO��ƽ��ת����Ϊ$\frac{�仯��}{��ʼ��}��100%$=$\frac{0.24}{0.8}$��100%=60.0%���ʴ�Ϊ�����ȣ����ڣ�60.0%��
��4��a����ѹʱ���������г��뺤�����������Ũ�ȱ�С�����Է�Ӧ���ʼ�С������ȷ��
b������Ӧ�����ȷ�Ӧ�������¶ȣ���ѧƽ�������ƶ�������ȷ��
c������NO��Ũ�ȣ��൱������ѹǿ��ƽ�ⲻ�ƶ�������NO��ת���ʲ��䣬�ʴ���
d��ƽ�ⳣ�����¶ȵĺ�����������С�����������ƽ�ⳣ�����䣬�ʴ���ѡ��a��b��
���� ���⿼���˻�ѧƽ����жϡ���ѧƽ�ⳣ���ĺ����֪ʶ�㣬�ѶȲ���ѧƽ��״̬���ж��Ǹ߿����ȵ㣬ע�⻯ѧƽ�ⳣ��ֻ���¶��йأ��������������أ�


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д� Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A�� | �⻯��ķе㣺H2T��H2R | B�� | M��T�γɵĻ������������ | ||
| C�� | ������ϡ���ᷴӦ�����ʣ�L��Q | D�� | L2+��R2-�ĺ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ�Ǽ���ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺
��ͼ�Ǽ���ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ--��ɫƿ�������� | B�� | �����--��Ƥ��������ƿ | ||
| C�� | ����������--���ƿ��ú���� | D�� | ϡ����--ϸ��ƿ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʹ�õ���Ҫ�����������ƾ��ơ�������������Ȧ������̨ | |
| B�� | ��Һʱ����Һ©���е��²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� | |
| C�� | ����ʱ��������ĩ��Ӧ������������ֽ�� | |
| D�� | �ù��Ϊ10 mL����Ͳ��ȡ6.20 mL��Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
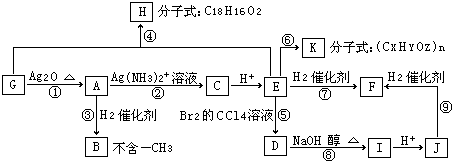
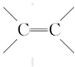 ��
��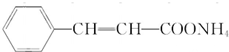 ������K�Ľṹ��ʽ
������K�Ľṹ��ʽ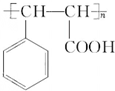 ��
��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������NaOHˮ��Һ��ϼ��� | |
| B�� | �״���Ũ�����ϼ��� | |
| C�� | �Ҵ���Ũ�����ϼ��� | |
| D�� | 2-�嶡����NaOH���Ҵ���Һ��ϼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | С�մ�����ᷴӦ��CO32-+2H+�TCO2��+H2O | |
| B�� | AlCl3��Һ�м��������İ�ˮ��Al3++3OH-�TAl��OH��3�� | |
| C�� | ���Ȼ�����Һ�м������� Fe3++Fe�T2Fe2+ | |
| D�� | ������������ǿ�Al��OH��3+OH-�TAlO2-+2H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com