
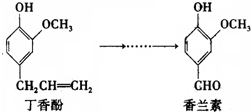
| A、香兰素分子中至少有12个原子共平面 |
| B、丁香酚不能与三氯化铁溶液发生显色反应 |
| C、1mol香兰素最多能与3mol氢气发生加成反应 |
| D、常温下1mol丁香酚只能与1molBr2反应 |


科目:高中化学 来源: 题型:
| A、改燃煤为燃气,可以减少废气中S02等有害物质的排放量天气的一种措施 |
| B、84消毒液的有效成分是NaClO |
| C、凡含有食品添加剂的食物对人体健康均有害 |
| D、金属防护中:牺牲阳极的阴极保护法利用的是原电池原理,外加电流的阴极保护法利用的是电解原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:


 )结构.
)结构.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液只能是CH3COONa溶液 |
| B、溶液中的离子浓度可能是c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、溶液中的离子浓度可能是c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、溶液中的离子浓度可能是c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,某溶液中水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、ClO-、SO42- |
| B、对N2(g)+3H2(g)?2NH3(g),恒温恒容时充入N2,正反速率增大,逆反应速率减小 |
| C、已知25℃时,Ksp(AgCl)=1.8×10-10,则在0.1mol-1AlCl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol?L-1 |
| D、在酸碱中和滴定时,装标准的滴定管未用标准液润洗直接装入标准液进行滴定,会引起测定结果浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ⅰ,① | B、Ⅱ,② |
| C、Ⅲ,③ | D、Ⅳ,④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取适量反应后的固体放入试管中, |

| SO2被氧化的程度 | V与m1或m2的关系 |
| 未被氧化 | |
| 完全被氧化 | V=0 |
| 部分被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、若铬比铁活泼,则电子经外电路由铁电极流向铬电极 |
| B、若铬比铁活泼,则铁电极反应式为2H++2e-=H2↑ |
| C、若铁比铬活泼,则溶液中H+向铁电极迁移 |
| D、若铁电极附近溶液pH增大,则铁比铬活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com