
【题目】以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下所示。

(1)形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___________。
(2)Ni2O3有强氧化性,加压酸浸时有气体产生且镍被还原为Ni2+,则产生的气体为______(填化学式)。
(3)滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体时所有反应的离子方程式:__________________________,_________________________。
(4)已知:3Fe2++2[Fe(CN)6]3-==Fe3[Fe(CN)6]2↓(蓝色沉淀);4Fe3++3[Fe(CN)6]4-==Fe4[Fe(CN)6]3↓(蓝色沉淀)。下列可以用于检验滤液C中金属阳离子的试剂有____________(填标号)
a.KSCN溶液 b.K3[Fe(CN)6] c.K4[Fe(CN)6] d.苯酚
(5)兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金。碱浸镍铝合金后,残铝量对兰尼镍的催化活性有重大影响,根据下图分析,残铝量在_____范围内催化活性最高,属于优质产品。

(6)仿照下面示例,设计从浸出液E回收氧化铝的流程:浸出液E_________________。
(示例:![]() )
)
【答案】 0 O2 H2S+2Fe3+==2Fe2++2H++S↓ H2S+Ni2+==Ni↓+2H++S↓ b 4%~6% ![]()
【解析】(1)Ni(CO)4中碳为+2价、氧-2价,故Ni的化合价为0;(2)Ni2O3有强氧化性,加压酸浸时有气体产生且镍被还原为Ni2+,Ni的化合价降低,则氧元素的化合价应升高,则产生的气体为O2;(3)滤渣D为单质镍、硫的混合物,浸出液B含有Fe3+、Ni2+,向其中通入H2S气体时Fe3+被还原为Fe2+,同时生成硫单质,且Ni2+被还原为单质,反应的离子方程式:H2S+2Fe3+==2Fe2++2H++S↓、H2S+Ni2+==Ni↓+2H++S↓;(4)根据上述分析,过滤后得到滤液C含有Fe2+,检验滤液C中金属阳离子的试剂可选择.K3[Fe(CN)6],答案选b;(5)根据下图分析,残铝量在4%~6%范围内催化活性最高,属于优质产品;(6)从浸出液E回收氧化铝的流程可表示为:浸出液E![]() 。
。


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A. c1∶c2=3∶1 B. 平衡时,Y和Z的生成速率之比为2∶3
C. X、Y的转化率不相等 D. c1的取值范围为0<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法不正确的是
A. 1mol甲基(-CH3)中含有的电子数为9NA
B. 标准状况下,22.4LCH2=CH2中含C-H数为4NA
C. 1mol分子式为C2H6O的物质,含O-H数一定是NA
D. 0.1mol由乙烯与乙醇组成的混合物完全燃烧所消托的氧气分子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡(SnCl4) 用作媒染剂和有机合成上的氯化催化剂。实验室制备四氯化锡的装置如下图(部分夹持装置已略去),已知:①金属锡熔融时通入干燥氯气反应可生成四氯化锡;② 无水四氯化锡熔点-33℃,沸点114.1℃;③无水四氯化锡遇水蒸气生成白色烟雾。下列说法不正确的是
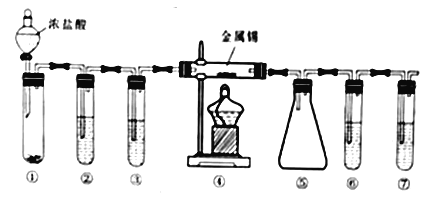
A. 实验时滴加浓盐酸反应一段时间,然后再点燃④处的酒精灯
B. ①、②、⑥、⑦的试管中依次盛装MnO2、饱和食盐水、浓H2SO4、NaOH溶液
C. ⑤装置用于收集SnCl4,浸泡在冷水浴中效果更好
D. ⑥、⑦两个试管可以用一个装有碱石灰的干燥管来代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类、归纳等是化学学习常用方法。下列分类、归纳正确的是
A.氧化物:SO2、HClOB.复合肥料:KNO3、CO(NH2)2
C.人体必需微量元素:Ca、SeD.有机物:C6H12O6、CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能层与能级的说法中正确的是( )
A. 同一原子中,符号相同的能级,其上电子能量不一定相同
B. 任一能层的能级总是从s能级开始,而且能级数不一定等于该能层序数
C. 同是s能级,在不同的能层中所能容纳的最多电子数是不相同的
D. 多电子原子中,每个能层上电子的能量一定不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某公司设计的用于驱动潜艇的液氨﹣液氧燃料电池示意图如下,有关说法正确的是( )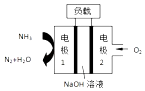
A.电池总反应为:4NH3+3O2=2N2+6H2O
B.电池工作时,OH﹣向正极移动
C.电极 2 发生的电极反应为:O2+4H++4e﹣=2H2O
D.电流由电极 1 经外电路流向电极2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下体积不变的密闭容器中:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=-905.9k/mol,下列叙述正确的是
4NO(g)+6H2O(g) △H=-905.9k/mol,下列叙述正确的是
A. 4molNH3和5molO2反应,达到平衡时放出的热量为905.9kJ
B. 平衡时V正(O2)=4/5V逆(NO)
C. 适当增大氧气的浓度可以提高氨气的转化率
D. 降低压强,正反应速率减小,逆反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期系的叙述正确的是 ( )
A. 元素周期系中ⅠA族元素又称为碱金属元素
B. 元素周期系中每一周期元素的种类均相等
C. 元素周期系的形成原因是核外电子排布的周期性变化
D. 每一周期的元素最外层电子数均是1→8,周而复始
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com