
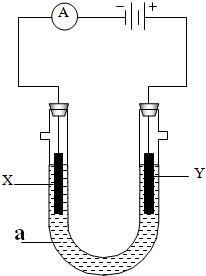
 ʹ����ͼ��ʾװ�ý��е��ʵ�飬����X��Y��Ϊʯī�缫��U�ι���ʢ��200mL��Һa���Իش��������⣺
ʹ����ͼ��ʾװ�ý��е��ʵ�飬����X��Y��Ϊʯī�缫��U�ι���ʢ��200mL��Һa���Իش��������⣺
| ||
| ||
| 0.64g |
| 64g/mol |
| 0.02mol |
| 0.2L |


 Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| x |
| y |
| x |
| y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 �����������Ҫ���о���Ӧ�ü�ֵ��
�����������Ҫ���о���Ӧ�ü�ֵ��| ���� |
| ��� | ���� | ���� | ���� | |
| �¶�/�� | ���� | |||
| 1 | 40 | FeCl3��Һ | ||
| 2 | 20 | FeCl3��Һ | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | �� | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ϊ̽��NH3���ܽ��ԣ�ij��ȤС�鰴��ͼ��ʾװ�ý���ʵ�飨fΪֹˮ�У�����ش��������⣺
Ϊ̽��NH3���ܽ��ԣ�ij��ȤС�鰴��ͼ��ʾװ�ý���ʵ�飨fΪֹˮ�У�����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1�������£�������ؾ�����Ũ���������һ�����壬������������仯ѧ���������ȷ��ֵġ���ͼ��ʾ����Ũ����С�ĵ���Y�ι�B�ˡ�
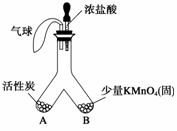
�ٿ�ʼ�۲쵽���������������������������������������������������� ��
��һ��ʱ����ֿɹ۲쵽�������� �������� ���������һ�������������������������������������������������������������������������������� ��
��Ӧ�û���̿�Ĵ����ʿ������������� ���������ﵽ������������Ŀ�ģ���һ�����ɣ���
��2����д��CO2��Na2O2��Ӧ�Ļ�ѧ����ʽ������������������������������ ��
��ijѧ���ж�SO2��Na2O2��Ӧ�����������ƣ�����Ϊ�����жϺ��������������������������� ��
��Ҫ˵�����ɣ��� ����������������������������������������������������������������������������������
�۸�ͬѧ���϶���Ӧ���Ƿ����������ɣ���ʹ����ͼ��ʾװ�ý���ʵ�飨ͼ������̨��װ������ȥ����
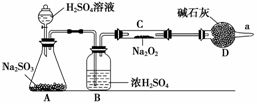
װ����B�������� ����������������������������������������������������������������������������������
D�������� �������������������������������������������������������������������������������������� ��
�����֤����ͬѧ�������ƶϣ� ����������������������������������������������������������������������
������������������������������������������������������������������������������������������������ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com