
按要求回答下列问题。
(1)SO2是形成酸雨的罪魁祸首。 64 g SO2的物质的量为 ,在标准状况下的体积约为 ,所含原子数为 。
(2)写出除去下列物质所含杂质(括号内为杂质)所用的试剂或方法:
①Na2CO3固体(NaHCO3) ②FeCl3溶液(FeCl2)
③Mg粉(Al) ④CO2(SO2)
(1)1 mol , 22.4L , 3NA或1.806×1024
(2)①加热 ②Cl2 ③NaOH溶液(或KOH溶液) ④KMnO4(H+)溶液(或饱和NaHCO3溶液)
解析试题分析:(1)根据物质的理和质量,体积,微粒数的关系进行计算即可。(2)①Na2CO3固体(NaHCO3)由于后者能加热分解生成碳酸钠,故用加热法。②FeCl3溶液(FeCl2)Cl2能和氯化亚铁反应生成氯化铁。③Mg粉(Al)可加入强碱溶液进行过滤即可。④CO2(SO2)由于二氧化硫具有还原性或酸性较二氧化碳强,故可以选择KMnO4(H+)溶液(或饱和NaHCO3溶液)。
考点:本题考查物质的量与各量的间的转化计算及物质的除杂方法。


科目:高中化学 来源: 题型:填空题
硫、氮、碳、铁、铜等常见元素在化合物中常表现出多种价态,如硫有-2、-1、+2、+4、+6等价态。这些元素在化工生产中有着重要应用。
(1)31.2g镁与碳粉的混合物在一定条件下恰好完全反应,再加入足量水,得到40.6g白色沉淀,同时产生密度为1.4107g/L(标准状况)的丙二烯和不饱和烃X的混合气体。
①镁与碳粉的反应产物的化学式为 ______________ 。
②原混合物中碳粉的物质的量分数为 ___________。(用小数表示,保留2位小数)
(2)某复杂盐由三种元素组成,含两种阳离子和两种阴离子。取21.76g该复杂盐,平均分为两份。将第一份溶于足量盐酸酸化的氯化钡溶液,所得沉淀中含9.32g硫酸钡。将第二份溶于足量热浓硝酸,再滴加足量硝酸钡溶液,得13.98g白色沉淀,过滤后向蓝色滤液中加足量烧碱溶液,过滤、洗涤、灼烧,得8.00g黑色固体。
①该复杂盐的化学式为_____________。
②该复杂盐中两种阳离子的质量比为 _________________ 。
(3)某地质学家经勘测发现一种新的磁黄铁矿,主要成分为Fe1-xS1+x,杂质不含Fe、S。分析可知该磁黄铁矿中,铁元素中三价铁的质量分数为75%。取5吨 73%的该磁黄铁矿,用接触法制硫酸,若沸腾炉中煅烧的损耗率为4%,接触室中反应的转化率为94%,SO3的吸收效率为97%,则最多可制得98.3%的浓硫酸的质量是________________。(保留2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某混合物的水溶液,可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32—、SO42—,现分别取100 mL的两等份溶液进行如下实验:
①第一份加过量NaOH溶液后加热,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,沉淀经足量盐酸洗涤、干燥后,得到11.65 g固体。
(1)一定不存在的离子是________(填离子符号,下同)。
(2)由①可知存在离子为________,浓度________。由②可知存在离子为________,浓度________。
由③可知存在离子为________,浓度________。
(3)K+是否存在?________(填“是”或“否”),理由是___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶某品牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含25% NaClO、1 000 mL、密度1.19 g·cm-3,稀释100倍(体积比)后使用。
请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为_____mol·L-1。
(2)该同学取100 mL该品牌“84消毒液”稀释后用于消毒,稀释后的溶液中
c(Na+)≈_____mol·L-1(假设稀释后溶液密度为1.0 g·cm-3)。
(3)该同学参阅该品牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25% NaClO的消毒液。下列说法正确的是_____。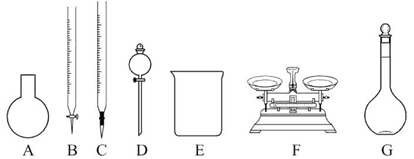
| A.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制 |
| C.利用购买的商品NaClO来配制可能导致结果偏低 |
| D.需要称量的NaClO固体质量为143 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)下列实验操作或对实验事实的描述不正确的是________(填序号)。
A.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
B.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大
C.分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出
D.用托盘天平称量11.74 g氯化钠晶体
E.用结晶法分离硝酸钾和氯化钠的混合物
(2)实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中配制溶液肯定不需要的是________(填序号);配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。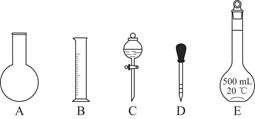
②下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
③请计算需用托盘天平称取固体NaOH的质量为________g。某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图。由图中可以看出,烧杯的实际质量为________g。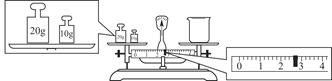
④根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据下列数据确定元素X的相对原子质量。
(1) 1.01×105 Pa,273 ℃时气态单质Xn的密度为d g/L,则X的相对原子质量为_____。
(2)相同状况下,一定体积的X的气态氢化物HmX的质量是等体积NH3的2倍。则X的相对原子质量为_____。
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)环境专家认为可以用铝将水中的NO3﹣ 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH﹣、Al(OH)3、NO3﹣、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
NO3﹣+ + → + + ﹣ 该反应过程中,被氧化与被还原的元素的物质的量之比为 .
(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=﹣a KJ/mol
Fe2O3(s)+C(s)=CO2(g)+2Fe (s)△H="+b" KJ/mol
C(s)+O2(g)=CO2(g)△H=﹣c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: .
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为 L(标准状况)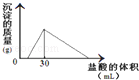
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)相同物质的量的O2和O3,所含分子数目之比为_______,所含氧原子的物质的量之比为_________。
(2)在标准状况下,①4 g H2.②11.2 L O2.③1 mol H2O中,含原子数最多的是_ ___,体积最小的是_______。(填序号)
(3)标况下,将224L的HCl气体溶于835ml(ρ=1g/cm3)的水中,所得盐酸的密度为1.2g/cm3, 该盐酸的物质的量浓度___________.。
(4)某气体物质质量为6.4 g,含有6.02×1022个分子,则该气体的相对分子质量为_______。
(5)Na2CO3的摩尔质量是____________,0.5mol Na2CO3的质量是____________,含有________mol Na+,Na+的个数约为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com