
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈(填“酸性”、“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO-)(填“>”、“=”或“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(Na+) c(CH3COO-)。
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。
(5)pH相同的氨水和氢氧化钠溶液,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的pH仍相同,则m________n(填“>”、“<”或“=”);
(1)碱性,>; (2)酸性,<;
(3)中性,>; (4)<,>。 (5)>
【解析】
试题分析:(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,得到醋酸钠溶液,醋酸根离子水解,使溶液成碱性;所以钠离子的浓度大于醋酸根离子的浓度;
(2)pH=3的醋酸和pH=11的氢氧化钠溶液中氢离子的浓度等于氢氧根离子的浓度,但醋酸是弱酸,所以醋酸溶液的浓度大于氢氧化钠溶液的浓度,等体积混合时醋酸过量,则溶液呈酸性;因为醋酸过量,溶液呈酸性,所以c(Na+)<c(CH3COO-);
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,根据电荷守恒定律,则c(OH-)= c(H+),所以溶液呈中性;若二者等体积混合,则溶液呈碱性,所以呈中性时,醋酸稍多,则醋酸体积>氢氧化钠溶液的体积;
(4)醋酸与氢氧化钠混合后溶液呈中性,若氢离子的浓度与氢氧根离子的浓度相等,则等体积混合时,醋酸过量,所以溶液呈酸性,现在溶液呈中性,则醋酸溶液中c(H+)<氢氧化钠溶液中c(OH-);若溶液的浓度相等,则溶液呈碱性,所以等体积混合时,醋酸的浓度大于氢氧化钠的浓度,m>n;
(5)pH相同的氨水和氢氧化钠溶液,分别用蒸馏水稀释至原来体积的m倍和n倍,若稀释倍数相同,因为氨水中还存在电离平衡,则稀释相同倍数后,氨水的pH>氢氧化钠溶液;现在稀释后两溶液的pH仍相同,所以氨水需再加水稀释,则氨水的稀释倍数m>氢氧化钠溶液的稀释倍数n。
考点:考查溶液的浓度、离子浓度、pH之间关系的判断,溶液稀释的判断


科目:高中化学 来源:2014-2015学年山东省滕州市高三1月月考理综化学试卷(解析版) 题型:填空题
(选考)【化学—选修5:有机化学基础】(15分)
有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:

已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
③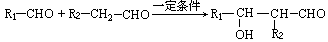
回答以下问题:
(1)A中含有的官能团名称是 。
(2)写出有机反应类型B→C ,F→G ,I→J 。
(3)写出F生成G的化学方程式 。
(4)写出J的结构简式 。
(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式。
①FeCl3溶液发生显色反应
②能发生银镜反应
③苯环上只有两个对位取代基
④能发生水解反应 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:选择题
下表是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和是2l。下列说法不正确的是

A.原子半径Z>W>Y
B.最高价氧化物对应水化物的酸性Z>W
C.氢化物的稳定性X>Z
D.X的氢化物与Y的氢化物能发生化合反应生成离子化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
(16分)以下是对化学反应变化过程及结果的研究。按要求回答问题:
(1)已知:
甲醇脱水反应①2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
甲醇制烯烃反应②2CH3OH(g)=C2H4 (g)+2H2O(g) ?△H2=-29.1kJ·mol-1
乙醇异构化反应③CH3CH2OH(g)=CH3OCH3(g)+H2O?△H3=+50.7kJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的△H= 。
(2)在25℃下,将pH=a的氢氧化钠溶液与pH=b的醋酸溶液等体积混合,若两溶液恰好完全反应,则a+b________14(填“>”、“<”或“=”);该温度下醋酸的电离常数K=__________(用含a、b的式子表示)。
(3)用一个离子方程式表示反应:100ml 3mol·L-1NaOH溶液中通入标准状况下4.48LCO2 ;所得溶液中离子浓度大小排列顺序为: ;
(4)废氨水可以转化成氨,氨再设计成碱性燃料电池。下图是该燃料电池示意图,产生的X气体可直接排放到大气中。

a电极电极反应式为 ;T℃下,某研究员测定NH3·H2O的电离常数为1.8×10-5,NH4+的水解平衡常数为1.5×10-8(水解平衡也是一种化学平衡,其平衡常数即水解常数),则该温度下水的离子积常数为 ,请判断T 25℃(填“>”“<”“=”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:选择题
关于如图装置说法正确的是

A.装置①中,盐桥中的K+移向ZnSO4溶液
B.装置②工作一段时间后,a极附近溶液的OH-的浓度增大
C.用装置③精炼铜时,c极为粗铜
D.装置④中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
将6molA和2molB在2L的密闭容器中混合并在一定条件下发生如下反应:3A(g)+B(S) 2C(g) ΔH<0,4s(秒)后反应达到平衡状态,此时测得C的浓度为1mol·L-1,下列说法中正确的是
2C(g) ΔH<0,4s(秒)后反应达到平衡状态,此时测得C的浓度为1mol·L-1,下列说法中正确的是
A.4s内用物质B表示的反应速率为0.125mol·L-1·S-1
B.达到平衡后若向容器中通入惰性气体,则A的转化率增大
C.此时,A、B、C的物质的量之比为3:1:2
D.达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
实验室中制取、洗气并收集气体的装置如图所示。仅用此该装置和表中提供的物质完成相关实验,最合理的选项是
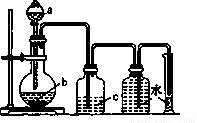
选项 | a中的液体 | b中的固体 | c中液体 |
A | 浓盐酸 | MnO2 | 饱和食盐水 |
B | 浓氨水 | 生石灰 | 浓H2SO4 |
C | 浓硫酸 | Cu片 | NaOH溶液 |
D | 稀HNO3 | Cu片 | H2O |
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
对下列各溶液中,微粒的物质的量浓度关系表述正确的是
A.0.1 mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B.0.1 mol/L的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-)
C.将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.在25℃100 mL NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列物质中,既能导电又属于电解质的是
A.蔗糖 B.熔融的氯化钠 C.氯化氢气体 D.锌片
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com