
【题目】如图所示,是原电池的装置图。请回答:
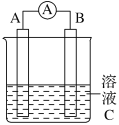
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为____________;
(2)若需将反应:Cu+2Fe3+===Cu2++2Fe2+设计成如上图所示的原电池装置,则A(负极)极材料为______,B(正极)极材料为________,溶液C为________。
(3)若C为CuCl2溶液,Zn是________极,Cu电极反应为_________________。反应过程溶液中c(Cu2+)________(填“变大”“变小”或“不变”)。
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
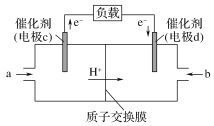
电池总反应为2CH3OH+3O2===2CO2+4H2O,则c电极是________(填“正极”或“负极”),c电极的反应方程式为________。若线路中转移2 mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为________L。
【答案】2H++2e-=H2↑ 铜 C FeCl3溶液 负 Cu2++2e-=Cu 变小 负极 H2O+CH3OH-6e-=CO2+6H+ 11.2
【解析】
利用原电池的工作原理,进行分析判断;
(1)C为稀硫酸,电流表指针发生偏转,B电极材料为Fe,且作负极,A电极为正极,总电极反应式为Fe+2H+=Fe2++H2↑,即A电极反应式为2H++2e-=H2↑;
答案为2H++2e-=H2↑;
(2)根据原电池工作原理,以及总电极反应式,负极材料是Cu,正极材料是石墨,溶液C为FeCl3;
答案为Cu;石墨;FeCl3溶液;
(3)Zn比Cu活泼,Zn为负极,锌电极反应式为Zn-2e-=Zn2+,Cu为正极,Cu电极反应式为Cu2++2e-=Cu,整个过程中Cu2+被消耗,即c(Cu2+)变小;
答案为负极;Cu2++2e-=Cu;变小;
(4)根据装置图,电子从电极c流向电极d,因此电极c为负极,燃料电池中通燃料一极为负极,即CH3OH在负极上失去电子,其电极反应式为H2O+CH3OH-6e-=CO2+6H+,消耗1molO2需要得到4mole-,因此电路中转移2mol电子,消耗氧气的物质的量为![]() =0.5mol,标准状况下,消耗氧气的体积为0.5mol×22.4L·mol-1=11.2L;
=0.5mol,标准状况下,消耗氧气的体积为0.5mol×22.4L·mol-1=11.2L;
答案为负极;H2O+CH3OH-6e-=CO2+6H+;11.2L。


科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是
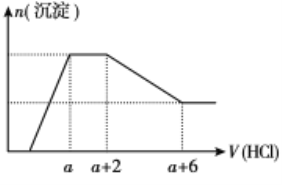
A. 原溶液中一定含有Na2SO4
B. 反应后最终溶液中的溶质只有AlCl3
C. 原溶液中含有CO32-与AlO2-的物质的量之比为1:1
D. 原溶液中一定含有的阴离子是OH-、SiO32-、AlO2-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列相关化学用语表述正确的是( )
A. NH4Cl的电子式: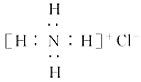
B. C原子的轨道表示式: ![]()
C. 冰醋酸为共价化合物,受热熔融:CH3COOH![]() CH3COO-+H+
CH3COO-+H+
D. Fe2+基态核外电子排布式为1s22s22p63s23p63d6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,2.24 L乙醇中含有的氧原子数目为0.1NA
B.1 L 1mol/L的NaHCO3溶液中Na+、H+和CO32-的数目均为NA
C.16 g的O2和O3混合气体中所含原子总数为NA
D.18 g水中所含电子总数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应2Fe3++2I-2Fe2++I2设计成如下图所示的原电池。

下列说法不正确的是( )
A.盐桥中的K+移向FeCl3溶液
B.反应开始时,乙中石墨电极上发生氧化反应
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某种原子的质量是a g,若NA只表示阿伏伽德罗常数的数值,该原子的相对原子质量为______,b g该原子的物质的量为______mol。
(2)a g A气体与b g B气体分子数相等,同温同压下,气体A与气体B的密度之比为___________。
(3)向10 mL 0.1mol/LNaHCO3溶液中缓缓滴入0.1mol/LCa(OH)2溶液,首先发生反应的两种离子为____________(填离子符号,下同),随后溶液中有白色沉淀生成,生成沉淀的两种离子为____________。当加入少量Ca(OH)2溶液时,发生的离子反应方程式为_______________________。
(4) 将3.22 g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需加入水的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不列离子方程式书写正确的是
A. 铜片与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO2↑+4H2O
B. 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C. 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
D. 用浓氢氧化钠溶液检验溶液中的NH4+:NH4++OH-![]() NH3·H2O
NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化锌常用作有机合成的催化剂。实验室采用HCl气体除水、ZnCl2升华相结合的方法提纯市售氯化锌样品(部分潮解并含高纯高温不分解杂质)。实验装置如图所示:
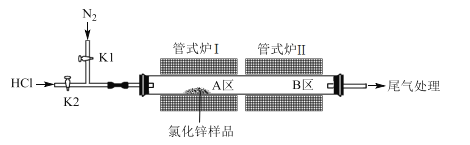
回答下列问题:
(1)无水氯化锌在空气中易潮解生成Zn(OH)Cl的化学方程式为_____。
(2)除水阶段:打开K1,K2。将管式炉I、II升温至150 ℃,反应一段时间后将管式炉I、II的温度升至350 ℃,保证将水除尽。除水阶段发生反应的化学方程式为 ____。
(3)升华阶段:撤去管式炉II,将管式炉I迅速升温至750℃,升温的目的是_____。一段时间后关闭管式炉I并关闭 ____(填K1或K2),待冷却后关闭 ____(填K1或K2)。最后将_____(填A或B)区的氯化锌转移、保存。
(4)除水阶段HCl与 N2流速要快,有利于提高除水效率。升华阶段HCl与N2流速要慢,其原因是_____。
(5)测定市售ZnCl2样品中的锌的质量分数。步骤如下:
① 溶液配制:称取m g样品,加水和盐酸至样品溶解,转移至250 mL的 ____中,加蒸馏水至刻度线,摇匀。
② 滴定:取25.00mL待测液于锥形瓶中,用c mol·L-1K4[Fe(CN)6]标准溶液滴定至终点,消耗V mL。滴定反应为:2K4[Fe(CN)6]+3ZnCl2=K2Zn3[Fe(CN)6]2↓+6KCl该样品中锌的质量分数为 ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 相同温度下,同时向①4mL0.1mol·L-1KMnO4酸性溶液和②4mL0.2mol·L-1KMnO4酸性溶液中,分别加入4mL1mol·L-1H2C2O4溶液 | ①中溶液先褪色 | 该实验条件下,KMnO4浓度越小,反应速率越快 |
B | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰,煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
C | 将苯、液溴和铁粉混合后,将产生的气体先通入CCl4,再通入水中,测所得水溶液的pH | pH<7 | 证明苯与液溴发生的是取代反应 |
D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com