
化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,某些反应与平衡常数数值如下:2NO(g) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g) 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g) 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
下列说法中正确的是
A.常温下,水分解产生O2,此时平衡常数的值约为5×10-80
B.常温下,最易分解放出O2的是水
C.
D.以上都不正确
科目:高中化学 来源:2014-2015宁夏银川市高一下学期3月月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.铜与稀硝酸反应:Cu+4H++2NO3-=Cu2++NO2↑+2H2O
B.醋酸溶液与碳酸氢钠溶液反应:H++HCO3-=H2O+CO2↑
C.氯气与烧碱溶液反应:Cl2+2OH-=Cl-+ClO-+H2O
D.硫酸溶液与氢氧化钡溶液反应:H++SO42-+OH-+Ba2+=H2O+BaSO4↓
查看答案和解析>>
科目:高中化学 来源:2014-2015内蒙古北方重工业集团三中高二下学期第一次月考化学试卷(解析版) 题型:选择题
乙醇分子中各种化学键如图所示。关于乙醇在下列反应中断键情况的说法中不正确的是

A.与金属钠反应时键①断裂
B.与乙酸发生酯化反应时键①断裂
C.与浓硫酸共热到170 ℃时键③、④断裂
D.在铜催化下与氧气反应时键①、③断裂
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:填空题
(12分)按要求回答下列问题:
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是 (填字母)
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中不变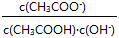
D.溶液中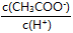 将减小
将减小
E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1:V2= (忽略溶液体积的变化)。
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是 (填字母)
A.若混合后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有:c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c(OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示:
溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①写出向NaClO溶液中通入少量CO2的离子方程式 。
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是 (填字母)
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)= (填准确数值)。
(4)已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析错误的是
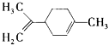
A.在一定条件下,1mol柠檬烯可与2molH2完全加成
B.柠檬烯的一氯代物有7种
C.在一定条件下,柠檬烯可发生加成、取代、氧化、还原反应
D.柠檬烯分子中所有碳原子不可能都在同一平面
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
用铂作电极电解某种溶液,通电一段时间后,溶液的pH变小,且在阳极得到0.56L气体,阴极得到1.12L气体(两种气体体积均在相同条件下测定)。由此可知,该溶液可能是
A.CuSO4溶液 B.HBr溶液 C.NaCl溶液 D.硫酸溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省高一3月月考化学试卷(解析版) 题型:填空题
(12分)某溶液可能含有K+、Mg2+、Al3+、Cl2、SO42-、S2-、NO3-中的几种,为确定溶液中的微粒种类,进行如下实验:
①通过观察,发现溶液呈浅黄绿色;
②取少许原溶液,滴加NaOH溶液直至过量,发现先有沉淀生成,后沉淀减少但并不完全消失;
③取少许原溶液,滴加BaCl2溶液,无白色沉淀生成。
请根据上述信息回答下列问题:
(1)原溶液中肯定存在上述微粒中的________________,肯定不存在的微粒有_______________。
(2)不能确定是否存在上述微粒中的______________________,确定其是否存在的实验方法是____________________(不要求写具体操作过程)。
(3)若步骤②中得到沉淀的最大质量为9.7g,最终剩余沉淀质量为5.8g,据此步骤可确定原溶液中一定存在的微粒的物质的量之比为____________________。
(4)下列离子还可以在原溶液中大量共存的是___________(填字母)。
A.OH- B.Fe2+ C.NH4+ D.CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:填空题
(10分)金属镁是六方最密堆积,金属铜是面心立方最密堆积,下图分别给出它们的堆积状况和晶胞示意图,它们空间利用率相同,假定镁、铜原子均为刚性小球,已知球的半径分别为R1厘米、R2厘米,阿伏伽德罗常数NA
| (1)镁原子在二维空间的配位数为 |
(2)位于晶胞中部的鎂原子与离它最近两平面 (填“相离”或“相切”或”相交”) | |
(3)请用含R1、NA的数学式子表达金属镁的密度: g/cm3(根号带在分子上) | |
| (4)铜原子在三维空间的配位数为 |
(5)晶胞中面心上的六个铜原子构成的空间几何体名称为 | |
(6)请用含R2、NA的数学式子表达金属铜的密度: g/cm3(根号带在分子上) |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年新疆乌鲁木齐地区高三第二次诊断性测试化学试卷(解析版) 题型:选择题
CH4和N2在一定条件下能直接生成氨:3CH4(g)+2N2(g)  3C(s)+4NH3(g)
3C(s)+4NH3(g) 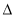 H>0,700 ℃时,
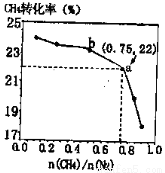
H>0,700 ℃时,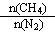 与CH4的平衡转化率的关系如图所示。下列判断正确的是
与CH4的平衡转化率的关系如图所示。下列判断正确的是
A.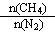 越大,CH4的转化率越高
越大,CH4的转化率越高
B.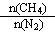 不变时,升温,NH3的体积分数会减小
不变时,升温,NH3的体积分数会减小
C.b点对应的平衡常数比a点的大
D.a点对应的NH3的体积分数约为13%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com