
为治理环境,减少雾霾,应采取措施减少二氧化硫、氮氧化物(NOx)等的排放量。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
②CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H2=-586.7kJ/mol
(1)若用4.48LCH4还原NO生成N2,则放出的热量为______kJ。(气体体积已折算为标准状况下)
Ⅱ.(2)NOx可用强碱溶液吸收产生硝酸盐。在酸性条件下,FeSO4溶液能将NO3-还原为NO,NO能与多余的FeSO4溶液作用生成棕色物质,这是检验NO3-的特征反应。写出该过程中产生NO的离子方程式: 。
(3)用电化学处理含NO3-的废水,电解的原理如图1所示。则电解时阴极的电极反应式为 ;当电路中转移20 mol电子时,交换膜左侧溶液质量减少________g。
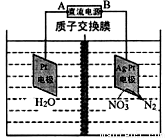
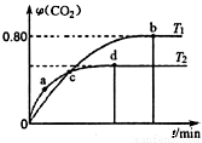
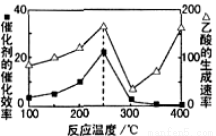
图1 图2 图3
Ⅲ.利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 molCO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 molCO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
(4)T1时,该反应的化学平衡常数的数值为 。
(5)下列说法不正确的是_______(填字母)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,在原容器中充入一定量氦气,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
Ⅳ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g)
CH3COOH(g) △H<0直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图3所示。
(6)①250~300℃时,乙酸的生成速率减小的主要原因是 。
②工业生产中该反应的温度常选择250℃、不选择400℃,从综合经济效益考虑,其原因是 。
科目:高中化学 来源:2016届宁夏银川二中高三三模理综化学试卷(解析版) 题型:选择题
下列离子方程式的书写正确的是
A.误将洁厕灵与消毒液混合:2H++Cl-+ClO-═Cl2↑+H2O
B.玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-═Na2SiO3↓+H2O
C.硝酸铝溶液中加入过量氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O
D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三下最后一次模拟理综化学试卷(解析版) 题型:填空题
[有机化学基础] 有机物H是一种重要的医药中间体。其结构简式如图所示:
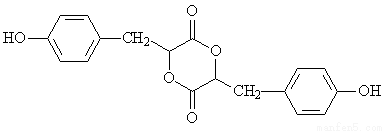
合成H的一种路线如下:
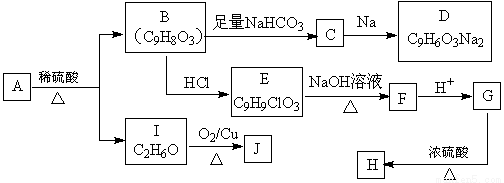
已知以下信息:
①有机物A遇氯化铁溶液发生显色反应,其分子中的苯环上有2个取代基,且A的苯环上一氯代物有2种。 ②J能发生银镜反应。
请回答下列问题:
(1)I的名称是 。G生成H的反应类型是 。
(2)B的含氧官能团名称是 ;E生成F的化学方程式为 。
(3)在一定条件下,A与J以物质的量比1∶1反应生成功能高分子材料K,K的结构简式为 。
(4)已知: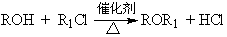 ,C与E以物质的量比1∶1混合在催化剂、加热条件下反应,写出化学方程式 。
,C与E以物质的量比1∶1混合在催化剂、加热条件下反应,写出化学方程式 。
(5)L是B的同分异构体,L符合下列条件的结构有 种(不考虑立体结构)。
①与B具有相同的官能团;②遇氯化铁溶液发生显色反应。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:实验题
Ⅰ.Fe3+具有氧化性,实验室测定含碘废液中I-的含量的过程如下:量取25.00 mL废液于250 mL锥形瓶中,分别加入5 mL 2 mol·L-1 H2SO4和10 mL 20% Fe2(SO4)3溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入几滴二苯胺磺酸钠(用作指示剂),用0.02500 mol·L-1标准K2Cr2O7溶液进行滴定到终点。重复3次,数据记录如下表:
次数 | 1 | 2 | 3 |
滴定体积/mL | 19.98 | 20.02 | 19.00 |
(1)在盛有废液的锥形瓶中先加入5 mL 2 mol·L-1 H2SO4的目的是
______________________________。(用离子方程式和语言叙述解释)
(2)上述过程中涉及的反应:①2Fe3++2I-===2Fe2++I2 ②______________________________。
(3)根据滴定有关数据,该废液中I-含量是_____g·L-1。
(4)在滴定过程中,下列操作(其他操作正确)会造成测定结果偏低的是___________。
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗衣后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡
Ⅱ.Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点。某学习小组同学设计如下实验:
实验编号 | 实验操作 | 现象 |
1 | 向10mL 3mol/L KNO3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 无白色沉淀生成 |
2 | 向10mL 1mol/L AgNO3溶液中滴加2mL 0.1mol/L FeSO4溶液,振荡,再滴加酸性KMnO4溶液 | 紫红色不褪去 |
3 | 向10mL 1mol/L Fe(NO3)3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 有白色沉淀生成 |
请回答:
(5)设计实验①的目的是______________________________。
(6)实验③可得出结论是______________________________。
(7)写出实验②中反应的离子方程式______________________________。
(8)根据以上实验,Fe3+和Ag+的氧化性相对强弱与离子____________________有关。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
2015年诺贝尔生理学或医学奖授予中国药学家屠呦呦以及爱尔兰科学家威廉·坎贝尔和日本科学家大村智,表彰他们在寄生虫疾病治疗研究方面取得的成就。屠呦呦先驱性地发现了青蒿素,开创了疟疾治疗新方法。右图为青蒿素,关于该物质的下列说法正确的是
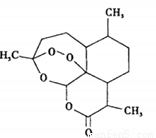
A.青蒿素化学式为C15H20O5
B.在光照条件下可能发生取代反应
C.可以与氢气发生加成反应
D.水浸青蒿对治疗疟疾有良好的疗效
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下学期冲刺模拟理综化学A卷(解析版) 题型:选择题
甲、乙分别是由同主族元素R、Z组成的两种单质,常温下能进行如下反应:甲+乙+H2O→HRO3+HZ(未配平)。下列说法不正确的是
A.制备1mol R转移电子数一定为2NA
B.R、Z简单离子的还原性:Z(离子)﹤R(离子)
C.HZ分子的稳定性大于HR分子
D.HRO3与HZ计量数之比为1:5
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:填空题
已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小。请回答:
(1)A、B、C、D的第一电离能由小到大的顺序是__________(用元素符号填空)
(2)化合物BD3的分子构型为__________,B的原子轨道杂化类型为__________。B元素氢化物的沸点低于其同族上周期元素的氢化物的原因是__________。
(3)己知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物.则F的基态原子价电子排布式为__________,CN-与__________(一种分子)互为等电子体.消除CN-剧毒性的方法之一是加入浓的双氧水,可将其转化为可溶性碳酸盐及氨气,写出该反应的离子方程式:__________。
(4)①E基态原子的价电子排布为__________,②EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为__________。
③已知该晶体的摩尔质量为M(g/mol),其中E4+的氧配位数为__________。若该晶胞边长为anm,可计算该晶体的密度为__________g/cm3(阿伏加德罗常数为NA)。

查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:选择题
硒(34Se)元素是人体必需的微量元素,它在自然界有六种核素。下列有关78Se和80Se的说法不正确的是
A.两者的质量数不同
B.两者的中子数不同
C.两者的核外电子数相同
D.两者互为同素异形体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中文科化学试卷(解析版) 题型:选择题
当光束通过下列分散系时,能产生丁达尔效应的是
A.CuSO4溶液 B.Na2CO3溶液 C.Fe(OH)3胶体 D.Ba(OH)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com