
在25 ℃时,用石墨电极电解2.0 L 2.5 mol·L-1CuSO4溶液,如有0.20 mol电子发生转移,请回答下列问题:
(1)阴极发生 反应,
电极反应式为 ;
(2)阳极发生 反应,
电极反应式为 ;
(3)电解后得到的铜的质量是 ,得到氧气的体积是 (标准状况),溶液的pH是 ;
(4)如果用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差 ,电解液的pH 。
(1)还原 2Cu2++4e-=2Cu
(2)氧化 4OH--4e-=2H2O+O2↑
(3)6.4 g 1.12 L 1
(4)12.8 g 不变
【解析】用石墨电极电解CuSO4溶液:
阳极反应式:4OH--4e-=2H2O+O2↑,
阴极反应式:2Cu2++4e-=2Cu。
当线路中有0.20 mol电子转移时,析出铜的质量为
m(Cu)=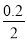 mol×64 g·mol-1=6.4 g。
mol×64 g·mol-1=6.4 g。
产生O2的体积
V(O2)=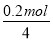 ×22.4 L·mol-1=1.12 L。
×22.4 L·mol-1=1.12 L。
c(H+)=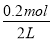 =0.1 mol/L,pH=-lg 0.1=1。
=0.1 mol/L,pH=-lg 0.1=1。
若用Cu片代替石墨电极,则该装置为电镀池,电解后溶液pH不变。当转移0.2 mol电子时,阳极溶解6.4 g,Cu阴极析出6.4 g Cu,则两极质量差为6.4+6.4=12.8(g)。


科目:高中化学 来源:2014年高中化学苏教版选修四模块综合检测练习卷(解析版) 题型:选择题
在一定条件下,将64 g二氧化硫气体氧化成三氧化硫气体时,实验测得放出热量为78.64 kJ,已知二氧化硫在此条件下的转化率为80%。下列热化学方程式书写正确的是( )
A.SO2(g)+ O2(g)
O2(g)  SO3(g) ΔH=-98.3 kJ·mol-1
SO3(g) ΔH=-98.3 kJ·mol-1
B.2SO2(g)+O2(g)  2SO3(l)ΔH=-196.6 kJ·mol-1
2SO3(l)ΔH=-196.6 kJ·mol-1
C.SO2(g)+ O2(g)
O2(g)  SO3(g)ΔH=-78.64 kJ·mol-1
SO3(g)ΔH=-78.64 kJ·mol-1
D.2SO2(g)+O2(g)  2SO3(g)ΔH=+196.6 kJ·mol-1
2SO3(g)ΔH=+196.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷(解析版) 题型:选择题
为了探究影响化学反应速率的因素,4位同学分别设计了下列4个实验,其中结论不正确的是( )
A.将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同
B.盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快
C.将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快
D.升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题1 化学反应与能量变化练习卷(解析版) 题型:选择题
[双选题]为了避免青铜器生成铜绿,以下方法正确的是( )
A.将青铜器放在银质托盘上
B.将青铜器保存在干燥的环境中
C.将青铜器保存在潮湿的空气中
D.在青铜器的表面覆盖一层防渗透的高分子膜
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题1 化学反应与能量变化练习卷(解析版) 题型:选择题
在钢铁腐蚀过程中,下列五种变化可能发生的是( )
①Fe2+转化为Fe3+ ②O2被还原 ③产生H2④Fe(OH)3失水形成Fe2O3·H2O
⑤杂质碳被氧化
A.只有①和② B.只有②③④
C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第四章 电化学基础练习卷(解析版) 题型:选择题
按下图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
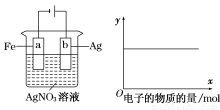
①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量
⑤溶液的pH
A.①③ B.③④ C.①②④ D.①②⑤
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第四章 电化学基础练习卷(解析版) 题型:选择题
如下图所示是某太空空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中正确的是( )
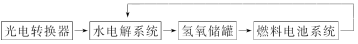
向日面时 背日面时
A.该能量转化系统工作时,需不断补充H2O
B.该转化系统的能量本质上来源于太阳能
C.水电解系统中的阴极反应:O2+2H2O+4e-=4OH-
D.燃料电池放电时的负极反应:H2-2e-=2H+
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第二章 化学反应速率与化学平衡练习卷(解析版) 题型:选择题
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
T/K | K1 | K2 |
973 | 1.47 | 2.38 |
1 173 | 2.15 | 1.67 |
下列有关叙述正确的是( )
A.b<0
B.在973 K下增大压强,K2增大
C.a>b
D.在常温下反应①一定能自发进行
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第一章 化学反应与能量练习卷(解析版) 题型:选择题
一些烷烃的燃烧热如下表:
化合物 | 燃烧热/kJ/mol | 化合物 | 燃烧热/kJ/mol |
甲烷 | 891.0 | 正丁烷 | 2878.0 |
乙烷 | 1560.8 | 异丁烷 | 2869.6 |
丙烷 | 2221.5 | 异戊烷 | 3531.3 |
下列表达正确的是( )
A.正戊烷的燃烧热大于3531.3 kJ/mol
B.稳定性:正丁烷<异丁烷
C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)ΔH=-1560.8 kJ/mol
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com