
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | Cl2+H2O═HC1+HC1O | D. | 2F2+2H2O═4HF+O2 |
分析 若水作还原剂,则水中O元素的化合价升高,以此来解答.
解答 解:A.2H2O$\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2中,水中H元素的化合价降低,O元素的化合价升高,则水既作氧化剂又作还原剂,故A错误;
B.2Na+2H2O═2NaOH+H2↑中,水中H元素的化合价降低,则水作氧化剂,故B错误;
C.Cl2+H2O═HC1+HC1O的反应中,Cl元素的化合价既有升高的又有降低的,水中的氢、氧元素的化合价都不变,所以氯气既是氧化剂又是还原剂,水既不是氧化剂又不是还原剂,故C错误;
D.2F2+2H2O═4HF+O2中,水中O元素的化合价升高,则水作还原剂,故D正确;
故选D.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化及还原剂的判断即可解答,题目较简单.


科目:高中化学 来源: 题型:实验题
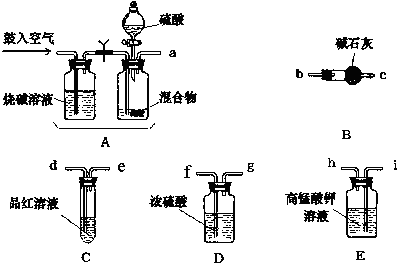
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 置换反应不一定全部是氧化还原反应 | |
| B. | 氧化还原反应中氧化剂和还原剂可以是同种物质 | |
| C. | 氧化反应和还原反应不一定同时发生 | |
| D. | 还原剂是得电子,氧化剂失电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只由一种元素的阳离子与另一种元素的阴离子组成的物质不一定是纯净物 | |
| B. | 用加热的方法可以除去混在NaCl固体中的NH4Cl,说明NH4Cl会升华 | |
| C. | SO2气体和Cl2均能使品红溶液褪色,说明两者均有强氧化性 | |
| D. | 浓硫酸不能用来干燥HI、CO、SO2等气体,因为浓硫酸具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
| C | 胆矾 | 氢氧化铁胶体 | 铁 | 碳酸钙 |
| D | 水银 | 澄清石灰水 | 氯化铜 | 碳酸钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
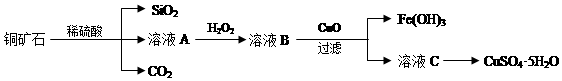
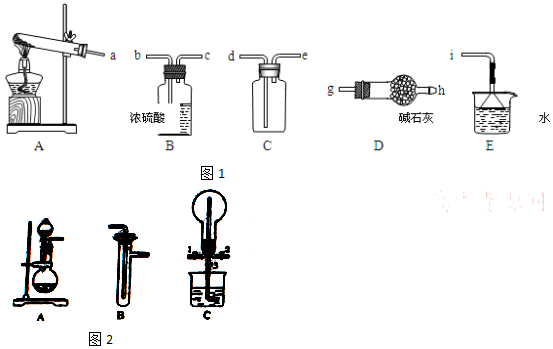
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
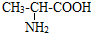 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
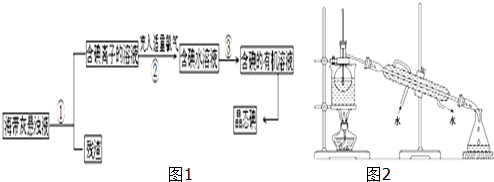
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com