
【题目】将SO2通入足量Fe2(SO4)3溶液中,完全反应后再加入K2Cr2O7溶液,发生的两个化学反应为①SO2+2Fe3++2H2O→![]() +2Fe2++W,②
+2Fe2++W,②![]() +aFe2++bH+→Cr3++Fe3++H2O。下列有关说法正确的是
+aFe2++bH+→Cr3++Fe3++H2O。下列有关说法正确的是
A.还原性:Cr3+>SO2B.方程式②中,a=6,b=7
C.![]() 能将Na2SO3氧化成Na2SO4D.方程式①中W为OH
能将Na2SO3氧化成Na2SO4D.方程式①中W为OH
【答案】C
【解析】
A、反应SO2+2Fe3++2H2O→SO42-+2Fe2++W中,SO2做还原剂,Fe2+为还原产物,所以还原性:SO2>Fe2+,反应Cr2O72-+aFe2++1bH+→Cr3++Fe3++H2O中,Fe2+为还原剂,Cr3+为还原产物,所以还原性:Fe2+>Cr3+,所以还原性:SO2>Cr3+,故A错误;
B、②Cr2O72-+aFe2++1bH+→Cr3++Fe3++H2O由得失电子守恒和电荷守恒配平方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,则a=6,b=14,故B错误;
C、重铬酸根具有氧化性,能将亚铁离子氧化,也能将Na2SO3 氧化成 Na2SO4,故C正确;
D、由方程式①电荷守恒,则W 为H+,故D错误。
故选:C。


科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
![]() 第一份加入
第一份加入![]() 溶液有沉淀产生;
溶液有沉淀产生;
![]() 第二份加足量NaOH溶液加热后,收集到气体
第二份加足量NaOH溶液加热后,收集到气体![]() ;
;
![]() 第三份加足量
第三份加足量![]() 溶液后,得干燥沉淀
溶液后,得干燥沉淀![]() ,经足量盐酸洗涤、干燥后,沉淀质量为
,经足量盐酸洗涤、干燥后,沉淀质量为![]() 根据上述实验,回答下列问题
根据上述实验,回答下列问题
(1)该溶液中一定存在的离子是______,可能存在的离子是______.
(2)求一定存在的离子中阳离子的浓度或浓度的取值范围______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是( )
A.![]() 和
和![]() 不属于同分异构体
不属于同分异构体
B.质量相同的![]() 和
和![]() 完全燃烧时消耗氧气的质量较少的是
完全燃烧时消耗氧气的质量较少的是![]()
C.连接四个不同基团的碳原子为“手性碳原子”,![]() 含有两个手性碳原子
含有两个手性碳原子
D.标准状况下![]() L溴乙烷所含化学键总数为
L溴乙烷所含化学键总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组探究足量的镁与浓硫酸反应。回答下列问题:
Ⅰ.甲同学设计如图实验验证该过程产生的混合气体中含有![]() 、
、![]() 。
。
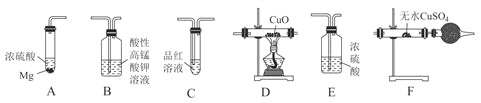
![]() 若按气体从左到右的流向,各装置的连接顺序是________
若按气体从左到右的流向,各装置的连接顺序是________![]() 填字母编号
填字母编号![]() 。
。
![]() 已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为________mol/L。
已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为________mol/L。
![]() 装置C的作用是________。
装置C的作用是________。
![]() 证明混合气体中含有H2的实验现象为________。
证明混合气体中含有H2的实验现象为________。
Ⅱ.乙同学设计如图实验测定混合气体中SO2的含量。

![]() 溶液可以是________
溶液可以是________![]() 填字母
填字母![]() 。
。
![]() 溶液
溶液
![]() 酸性
酸性![]() 溶液
溶液![]() 硫酸酸化
硫酸酸化![]()
![]() 溴水
溴水
![]() 步骤
步骤![]() 中洗涤沉淀的操作为________。
中洗涤沉淀的操作为________。
![]() 通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量
通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量![]() 体积分数
体积分数![]() 为________
为________![]() 用含V、m的代数式表示
用含V、m的代数式表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或描述中,正确的是
A.离子结构示意图  既可以表示35Cl-,也可以表示37Cl-
既可以表示35Cl-,也可以表示37Cl-
B.SO3的水溶液能导电,说明SO3是电解质
C.NaHSO3在水中的电离方程式:NaHSO3=Na++H++SO32-
D.同素异形体间的转化和同位素间的转化都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是
A.价电子排布为ns1的元素,不一定是s区元素
B.配合物Fe(CO)n内中心原子价电子数与配体提供电子总数之和为18,则n=5
C.光卤气(COCl2)、甲醛分子的立体构型和键角均相同
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是
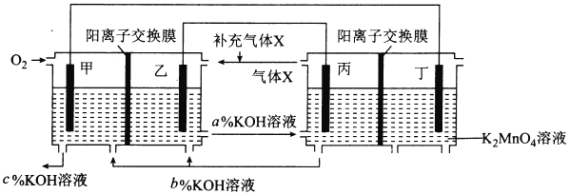
A. 甲为正极,丙为阴极
B. 丁极的电极反应式为MnO42――e-===MnO4-
C. KOH溶液的质量分数:c%>a%>b%
D. 标准状况下,甲电极上每消耗22.4L气体时,理论上有4molK+移入阴极区
查看答案和解析>>
科目:高中化学 来源: 题型:
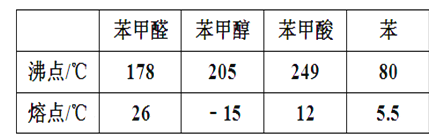
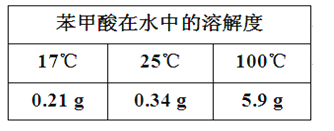
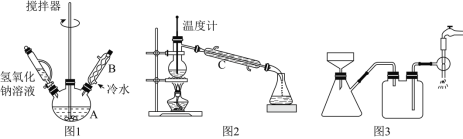
【题目】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲醇(在水中溶解度不大、易溶于有机溶剂,密度约等于水的密度)和苯甲酸。反应原理如下:2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa,C6H5COONa+HCl→C6H5COOH+NaCl。有关物质物理性质如表:
实验流程如下:

(1)第①步需连续加热1小时(如图1),其中加热和固定装置未画出。若将仪器B改为仪器C,效果不如B,说明原因__。
(2)操作中有关分液漏斗的使用不正确的是__。
A.分液漏斗在使用之前必须检查是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时等下层液体放完后立即关闭旋塞,换一个烧杯再打开旋塞使上层液体流下
(3)操作③用沸水浴加热蒸馏,再进行操作④(如图2),收集_℃的馏分。图2中有一处明显错误,正确的应改为__。
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体,__冲洗杯壁上残留的晶体,抽滤完成后洗涤晶体。
(5)用电子天平准确称取0.2440g苯甲酸样品于锥形瓶中,加100mL蒸馏水溶解(必要时可以加热),再用0.1000molL-1的标准NaOH溶液滴定,共消耗NaOH溶液19.20mL,则苯甲酸样品的纯度为__%(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)通入 CH3OH 电极的电极反应:___________________。
(2)乙池中 A(石墨)电极的名称为_________________(填“正极”、“负极”或“阴极”、“阳极”),总化学反应式为___________________。
(3)当乙池中 B 极质量增加 5.40g 时,甲池中理论上消耗 O2 的体积为_______mL(标准状况)。若丙池中KCl溶液的体积是500mL,电解后,溶液的pH为_________(设电解前后溶液体积无变化)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com