
| A. | 油脂制肥皂实验中加一定量的乙醇是为了增加油脂的溶解,加快反应速率 | |
| B. | 油脂制肥皂实验中加一定量的饱和食盐水为了降低肥皂的溶解度,使肥皂析出 | |
| C. | 反应过程中,混合液是否分层可以判断皂化反应是否完全 | |
| D. | 皂化反应的产物中都有甘油 |
分析 A.油脂难溶于水,在乙醇中的溶解度较大;
B.肥皂在氯化钠溶液中溶解度较小;
C.皂化反应的产物会混合在一起,不分层;
D.酯在碱性条件下的水解属于皂化反应.
解答 解:A.油脂难溶于水,在乙醇中的溶解度较大,油脂制肥皂实验中加一定量的乙醇是为了增加油脂的溶解,增大与碱的接触面积,加快反应速率,故A正确;
B.肥皂在氯化钠溶液中溶解度较小,所以油脂制肥皂实验中加一定量的饱和食盐水为了降低肥皂的溶解度,使肥皂析出,故B正确;
C.皂化反应的产物会混合在一起,不分层,所以反应过程中,混合液若不分层,则说明皂化反应已经完全,故C正确;
D.酯在碱性条件下的水解属于皂化反应,一般所说的皂化反应是油脂的碱性水解,所以并不是所有的皂化反应的产物中均有甘油,故D错误.
故选D.
点评 本题考查了油脂的性质及皂化反应,题目难度不大,侧重于基础知识的考查,注意把握油脂的结构与性质.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶液的物质的量浓度/mol•L-1 | 电离度/% | H+的物质的量浓度/mol•L-1 | pH |
| 0.1 | 2α | c1 | x |
| c | α | 2c1 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14g | B. | 47g | C. | 54g | D. | 94g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用①分离NaCl溶液和NaOH溶液 | |
| B. | 用②蒸干NH4Cl和饱和溶液获取NH4Cl晶体 | |
| C. | 用③配制100mL 0.1000mol•L-1 K2Cr2O2溶液 | |
| D. | 用④分离Na2CO3溶液和CH3COOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
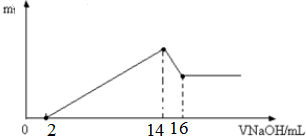
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丁的最高价氧化物可用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com