

 .
. 分析 (1)硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水;
(2)澄清石灰水中通入过量的CO2气体,反应生成碳酸氢钙;
(3)石灰石的主要成分为碳酸钙,碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水;
(4)氯化铁与铁反应生成氯化亚铁;
(5)铁与稀硫酸反应生成硫酸亚铁和氢气;
有化合价变化的属于氧化还原反应,没有不属于氧化还原反应,据此分析.
解答 解:(1)向H2SO4溶液中逐滴加入Ba(OH)2溶液,反应生成硫酸钡和水,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,没有化合价变化,不属于氧化还原反应,故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)澄清石灰水中通入过量的CO2气体,反应生成碳酸氢钙,反应的离子方程式为:CO2+OH-=HCO3-,没有化合价变化,不属于氧化还原反应,
故答案为:CO2+OH-=HCO3-;
(3)石灰石的主要成分为碳酸钙,碳酸钙与稀盐酸反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,没有化合价变化,不属于氧化还原反应,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(4)FeCl3溶液与Fe反应生成氯化亚铁,反应的离子方程式为:2Fe3++Fe═3Fe2+,Fe化合价升高,Fe3+化合价降低,转移电子数为2e-,
用双线桥标出电子转移的方向和数目为: 故答案为:
故答案为: ;
;
(5)Fe与稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑,Fe化合价升高,H+化合价降低,转移电子数为2e-,用双线桥标出电子转移的方向和数目为:
故答案为: .
.
点评 本题考查了离子方程式的书写及其用双线桥标出氧化还原反应电子转移的方向和数目,题目难度不大,明确发生反应的实质为解答关键,注意掌握离子方程式的书写原则,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋加入热水瓶中除去水垢 | ||
| C. | 蛋壳浸泡在白醋中有气体放出 | D. | pH试纸显示白醋的pH为2~3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中的还原剂为KNO3 | |
| B. | 该反应中C被还原 | |
| C. | 若消耗32gS,转移电子数为10mol | |
| D. | 若生成标准状况下气体22.4L,则有0.75 mol物质被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
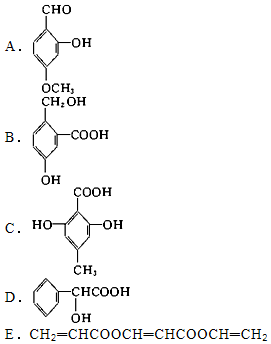
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物都是电解质 | |
| B. | 电解质一定是化合物 | |
| C. | SO2溶于水形的溶液能导电,所以SO2是电解质 | |
| D. | NaCl固体不导电,所以NaCl不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对不可回收垃圾常用的处理方法有卫生填埋、堆肥和焚烧 | |
| B. | 制造玻璃是复杂的物理变化,玻璃的组成不同,性能不同 | |
| C. | BaSO4在医学上用作钡餐 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的污染,且燃烧效率高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| B. | 含金属元素的离子一定是阳离子 | |
| C. | 金属单质只有还原性,金属阳离子不一定只有氧化性 | |
| D. | 不同的气体,若体积不同,则它们所含的分子数一定不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com