

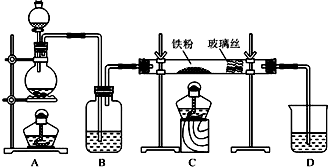
分析 该实验原理为:Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.通过测定CO2、H2O和N2的质量,确定分子中三种元素原子个数比,由此确定最简式,B中浓硫酸沉淀生成水的质量,C中碱石灰沉淀二氧化碳质量,D中铜网除去氧气,量气装置测定氮气体积.
(1)利用排水法测定氮气的体积,确定Wg该种氨基酸中含氮元素质量;
(2)防止氧气影响氮气体积的测定;
(3)除去氧气,防止影响氮气体积的测定;
(4)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素、N元素的质量,据此可以确定其原子个数比.若要确定分子式还需测定该氨基酸的相对分子质量.
解答 解:该实验原理为:Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.通过测定CO2、H2O和N2的质量,确定分子中三种元素原子个数比,由此确定最简式,B中浓硫酸沉淀生成水的质量,C中碱石灰沉淀二氧化碳质量,D中铜网除去氧气,量气装置测定氮气体积.
(1)装置的空气中含有N2,影响生成氮气的体积测定,需将装置中的N2排净,故答案为:将装置中的N2排净;
(2)最后测量生成氮气的体积,应先点燃D处酒精灯,防止未反应的氧气影响氮气体积的测定,故答案为:D;
(3)铜网的作用是吸收未反应的O2,保证最终收集到的气体是反应生成的N2,故答案为:吸收未反应的氧气,保证最终收集的是N2;
(4)该原理只能测出Wg该种氨基酸所含C元素、H元素、O元素、N元素的质量,据此可以确定其原子个数比,确定其最简式.若要确定分子式还需测定该氨基酸的相对分子质量,
故答案为:D.
点评 本题考查物质组成探究实验,掌握燃烧法根据原子守恒确定有机物分子组成,关键在于理解实验原理.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 相同条件下,与金属钠反应的速率,乙醇比乙酸慢 | |
| C. | 乙醇可由乙烯与水发生加成反应制得,乙酸可由乙醇氧化制得 | |
| D. | 乙醇和乙酸之间能发生酯化反应,酯化反应的逆反应为皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ③④⑤⑥ | B. | ①③④⑤ | C. | ①②③⑥⑦ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个Cl2在常温常压下体积约为22.4L | |
| B. | 在20℃、101kPa时,22.4L氢气中约含有2NA个氢原子 | |
| C. | 25℃、1.01×105Pa,48g SO2中含有的原子数为3NA | |
| D. | 22 g二氧化碳与标准状况下11.2LHCl含有相同的分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )| A. | a极为电池的正极 | |
| B. | b极发生氧化反应 | |
| C. | 负极的反应为:4H++O2+4e-═2H2O | |
| D. | 电池工作时,1mol乙醇被氧化时有12mol转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
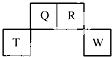 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,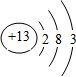 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com