
”¾ĢāÄæ”æĪŖĮĖĢ½¾æ»Æѧ·“Ó¦µÄČČŠ§Ó¦£¬Ä³ŠĖȤŠ”×é½ųŠŠĮĖČēĻĀŹµŃé£ŗ
£Ø1£©½«“æ¹ĢĢåĪļÖŹ![]() ·Ö±š×°ČėÓŠĖ®µÄ׶ŠĪĘæĄļ£Ø·¢Éś»Æѧ·“Ó¦£©£¬Į¢¼“Čū½ō“ųUŠĪ¹ÜµÄČū×Ó£¬·¢ĻÖUŠĪ¹ÜÄŚŗģÄ«Ė®µÄŅŗĆęø߶ČČēĶ¼ĖłŹ¾”£
·Ö±š×°ČėÓŠĖ®µÄ׶ŠĪĘæĄļ£Ø·¢Éś»Æѧ·“Ó¦£©£¬Į¢¼“Čū½ō“ųUŠĪ¹ÜµÄČū×Ó£¬·¢ĻÖUŠĪ¹ÜÄŚŗģÄ«Ė®µÄŅŗĆęø߶ČČēĶ¼ĖłŹ¾”£
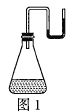

¢ŁČōČēĶ¼1ĖłŹ¾£¬·¢ÉśµÄ·“Ó¦£Ø¼ŁÉčƻӊĘųĢåÉś³É£©ŹĒ________£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©·“Ó¦£¬![]() ŹĒ________£ØĢīĮ½ÖÖĪļÖŹµÄ»ÆѧŹ½£©”£
ŹĒ________£ØĢīĮ½ÖÖĪļÖŹµÄ»ÆѧŹ½£©”£
¢ŚČōČēĶ¼2ĖłŹ¾£¬·¢ÉśµÄ·“Ó¦£Ø¼ŁÉčƻӊĘųĢåÉś³É£©ŹĒ________£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©·“Ó¦£¬ŅŌĻĀŃ”ĻīÖŠÓėĘäÄÜĮæ±ä»ÆĻąĶ¬µÄŹĒ________£ØĢīŠņŗÅ£©”£
A ![]() »¹Ō
»¹Ō![]() µÄ·“Ó¦ B
µÄ·“Ó¦ B ![]() µÄ·Ö½ā·“Ó¦ C
µÄ·Ö½ā·“Ó¦ C ![]() ŗĶ
ŗĶ![]() µÄ·“Ó¦
µÄ·“Ó¦
£Ø2£©ČēĶ¼3ĖłŹ¾£¬°ŃŹŌ¹Ü·ÅČėŹ¢ÓŠ25”걄ŗĶ³ĪĒåŹÆ»ŅĖ®µÄÉÕ±ÖŠ£¬ŹŌ¹ÜÖŠæŖŹ¼·Å¼øŠ”æéĀĮʬ£¬ŌŁµĪČė![]() Ļ”
Ļ”![]() ČÜŅŗ”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
ČÜŅŗ”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
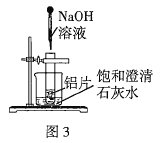
¢ŁŹµŃéÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ£ŗĀĮʬ֚½„Čܽā”¢ÓŠ“óĮæĘųÅŻ²śÉś”¢______”£
¢Ś²śÉśÉĻŹöĻÖĻóµÄŌŅņŹĒ___________”£
”¾“š°ø”æ·ÅČČ ![]() ”¢
”¢![]() »ņ
»ņ![]() £ØĢīĮ½ÖÖ¼“æÉ£© ĪüČČ B ±„ŗĶ³ĪĒåŹÆ»ŅĖ®ÖŠ³öĻÖ°×É«»ė×Ē ĀĮŗĶ
£ØĢīĮ½ÖÖ¼“æÉ£© ĪüČČ B ±„ŗĶ³ĪĒåŹÆ»ŅĖ®ÖŠ³öĻÖ°×É«»ė×Ē ĀĮŗĶ![]() ČÜŅŗ·“Ӧɜ³É
ČÜŅŗ·“Ӧɜ³É![]() £¬ĒŅøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬
£¬ĒŅøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬![]() µÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ų½µµĶ
µÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ų½µµĶ
”¾½āĪö”æ
Ķ¼1”¢2ĶعżUŠĪ¹ÜÄŚŗģÄ«Ė®±ä»Æ£¬ÅŠ¶ĻĢåĻµÄŚŃ¹ĒæÓėĶā½ē“óĘųŃ¹Ļą¶Ō“󊔣¬½ų¶ųÅŠ¶Ļ·“Ó¦µÄČČŠ§Ó¦£»Ģā£Ø2£©°ŃŹŌ¹Ü·ÅČėŹ¢ÓŠ25”걄ŗĶ³ĪĒåŹÆ»ŅĖ®µÄÉÕ±ÖŠ£¬ĻņŹŌ¹ÜÖŠ·ÅČė¼øŠ”æéĀĮʬ£¬ŌŁµĪČė![]() Ļ”
Ļ”![]() ČÜŅŗ£¬ĀĮŗĶ
ČÜŅŗ£¬ĀĮŗĶ![]() ČÜŅŗ·“Ӧɜ³ÉĒāĘų”£
ČÜŅŗ·“Ӧɜ³ÉĒāĘų”£
£Ø1£©¢ŁČōČēĶ¼1ĖłŹ¾£¬ĢåĻµÄŚŃ¹Ēæ“óÓŚĶā½ē“óĘųŃ¹£¬ĖµĆ÷ĢåĻµÄŚĘųĢåÅņÕĶ£¬·“Ó¦·ÅČČ£¬¹ŹĪļÖŹ![]() æÉŅŌŹĒ
æÉŅŌŹĒ![]() ”¢
Ӣ![]() Ӣ
”¢![]() µČ£»
µČ£»
¢ŚČōČēĶ¼2ĖłŹ¾£¬ĢåĻµÄŚŃ¹ĒæŠ”ÓŚĶā½ē“óĘųŃ¹£¬ĖµĆ÷ĢåĻµÄŚĘųĢåĢå»żĖõŠ”£¬·“Ó¦ĪüČČ£¬![]() »¹Ō
»¹Ō![]() µÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬
µÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬![]() µÄ·Ö½ā·“Ó¦ĪŖĪüČČ·“Ó¦£¬
µÄ·Ö½ā·“Ó¦ĪŖĪüČČ·“Ó¦£¬![]() ŗĶ
ŗĶ![]() µÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦”£“š°øŃ”B”£
µÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦”£“š°øŃ”B”£
£Ø2£©°ŃŹŌ¹Ü·ÅČėŹ¢ÓŠ25”걄ŗĶ³ĪĒåŹÆ»ŅĖ®µÄÉÕ±ÖŠ£¬ĻņŹŌ¹ÜÖŠ·ÅČė¼øŠ”æéĀĮʬ£¬ŌŁµĪČė![]() Ļ”
Ļ”![]() ČÜŅŗ£¬ĀĮŗĶ
ČÜŅŗ£¬ĀĮŗĶ![]() ČÜŅŗ·“Ӧɜ³É
ČÜŅŗ·“Ӧɜ³É![]() ĒŅøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬
ĒŅøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬![]() µÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ų½µµĶ£¬ÉÕ±ÖŠµÄ±„ŗĶ³ĪĒåŹÆ»ŅĖ®ÖŠ»į³öĻÖ°×É«»ė×Ē”£
µÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ų½µµĶ£¬ÉÕ±ÖŠµÄ±„ŗĶ³ĪĒåŹÆ»ŅĖ®ÖŠ»į³öĻÖ°×É«»ė×Ē”£


 æ¼Ē°±ŲĮ·ĻµĮŠ“š°ø
æ¼Ē°±ŲĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ŅŖĒóĢīæÕ£ŗ
£Ø1£©¾ßÓŠø“ŗĻ¹ŁÄÜĶŵÄø“ŌÓÓŠ»śĪļ£¬Ęä¹ŁÄÜĶžßÓŠø÷×ŌµÄ¶ĄĮ¢ŠŌ£¬ŌŚ²»Ķ¬Ģõ¼žĻĀĖł¾ßÓŠµÄ»ÆѧŠŌÖŹæÉ·Ö±š“Óø÷¹ŁÄÜĶÅĢÖĀŪ”£Čē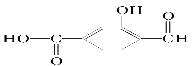 ¾ßÓŠČżÖÖ¹ŁÄÜĶÅ£ŗ______”¢__________ŗĶ__________(Ģī¹ŁÄÜĶŵÄĆū³Ę)£¬ĖłŅŌÕāøö»ÆŗĻĪļæÉæ“×÷______Ąą£¬______ĄąŗĶ______Ąą”£
¾ßÓŠČżÖÖ¹ŁÄÜĶÅ£ŗ______”¢__________ŗĶ__________(Ģī¹ŁÄÜĶŵÄĆū³Ę)£¬ĖłŅŌÕāøö»ÆŗĻĪļæÉæ“×÷______Ąą£¬______ĄąŗĶ______Ąą”£
£Ø2£©ōĒ»łµÄµē×ÓŹ½ŹĒ___________________________”£
£Ø3£©(CH3CH2)2C(CH3)2µÄĆū³ĘĪŖ_________________________”£
£Ø4£©2-¼×»ł-1£¬3-¶”¶žĻ©µÄ¼üĻߏ½___________________________”£
£Ø5£©![]() øĆÓŠ»śĪļ·¢Éś¼Ó¾Ū·“Ó¦ŗó£¬ĖłµĆ²śĪļµÄ½į¹¹¼ņĪŖ______”£
øĆÓŠ»śĪļ·¢Éś¼Ó¾Ū·“Ó¦ŗó£¬ĖłµĆ²śĪļµÄ½į¹¹¼ņĪŖ______”£
£Ø6£©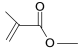 ·Ö×ÓŹ½ĪŖ_______________________½į¹¹¼ņŹ½ĪŖ______________________”£
·Ö×ÓŹ½ĪŖ_______________________½į¹¹¼ņŹ½ĪŖ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬ Õė¶Ō±ķÖŠµÄ¢Ł”«¢įÖÖŌŖĖŲ,ĢīŠ“ĻĀĮŠæÕ°×£ŗ
Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0×å |
1 | ¢Ł | |||||||
2 | ¢Ś | ¢Ū | ¢Ü | |||||
3 | ¢Ż | ¢Ž | ¢ß | ¢ą | ||||
4 | ¢į |
(1)Š“³öĻĀĮŠŌŖĖŲµÄŌŖĖŲ·ūŗÅ£ŗ ¢Ü_________”¢¢ą __________(Ģī¾ßĢåŌŖĖŲ·ūŗÅ£¬ĻĀĶ¬)£»¢ŻÕżŅ»¼ŪŃōĄė×ӵĽį¹¹Ź¾ŅāĶ¼ŹĒ________________”£
(2)×īøß¼ŪŃõ»ÆĪļŹĒĮ½ŠŌŃõ»ÆĪļµÄŌŖĖŲŹĒ___________£»ĖüµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÓė¢ŻµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_______________________________”£
(3)¢Ł”¢¢ŚĮ½ŌŖĖŲŠĪ³ÉµÄ×ī¼ņµ„»ÆŗĻĪļµÄ½į¹¹Ź½ĪŖ________________________£¬øĆ»ÆŗĻĪļŹĒÓÉ_________£ØĢī”°¼«ŠŌ”±”°·Ē¼«ŠŌ”±£©¼üŠĪ³ÉµÄ”£
(4)¢Ü¢ß¶žÖÖŌŖĖŲÖŠ·Ē½šŹōŠŌĒæµÄŹĒ___________”£
(5)¼ģŃéŌŖĖŲ¢įµÄ·½·ØŹĒ_______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ C”ŖC µ„¼üæÉŅŌČĘ¼üÖįŠż×Ŗ”£Ä³ĢžµÄ½į¹¹¼ņŹ½ČēĶ¼£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
![]()
A. øĆĢžŌŚŗĖ“Ź²ÕńĒāĘ×ÉĻÓŠ 6×éŠÅŗÅ·å
B. 1moløĆĢžĶźČ«Č¼ÉÕĻūŗÄ16.5mol O2
C. ·Ö×ÓÖŠÖĮÉŁÓŠ 10øöĢ¼Ō×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
D. øĆĢžŹĒ±½µÄĶ¬ĻµĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜŌ“Óė²ÄĮĻ”¢ŠÅĻ¢Ņ»Ęš±»³ĘĪŖĻÖ“śÉē»į·¢Õ¹µÄČż“óÖ§Öł”£Ćę¶ŌÄÜŌ“æŻ½ßµÄĪ£»ś£¬ĢįøßÄÜŌ“ĄūÓĆĀŹŗĶæŖ±ŁŠĀÄÜŌ“ŹĒ½ā¾öÕāŅ»ĪŹĢāµÄĮ½øöÖ÷ŅŖ·½Ļņ”£
(1)»Æѧ·“Ó¦ĖŁĀŹŗĶĻŽ¶ČÓėÉś²ś”¢Éś»īĆÜĒŠĻą¹Ų£¬ÕāŹĒ»ÆѧѧæĘ¹Ų×¢µÄ·½ĆęÖ®Ņ»”£Ä³Ń§ÉśĪŖĮĖĢ½¾æŠæÓėŃĪĖį·“Ó¦¹ż³ĢÖŠµÄĖŁĀŹ±ä»Æ£¬ŌŚ400mLĻ”ŃĪĖįÖŠ¼ÓČė×ćĮæµÄŠæ·Ū£¬ÓĆÅÅĖ®·ØŹÕ¼Æ·“Ó¦·Å³öµÄĒāĘų£¬ŹµŃé¼ĒĀ¼ČēĻĀ(ĄŪ¼ĘÖµ):
Ź±¼ä/min | 1 | 2 | 3 | 4 | 5 |
ĒāĘųĢå»ż/mL(±źæö) | 100 | 240 | 464 | 576 | 620 |
¢ŁÄÄŅ»¶ĪŹ±¼äÄŚ·“Ó¦ĖŁĀŹ×ī“ó£ŗ__________min(Ģī”°0”«1”±”°1”«2”±”°2”«3”±”°3”«4”±»ņ”°4”«5”±)”£
¢ŚĮķŅ»Ń§ÉśĪŖæŲÖĘ·“Ó¦ĖŁĀŹ·ĄÖ¹·“Ó¦¹żæģÄŃŅŌ²āĮæĒāĘųĢå»ż”£ĖūŹĀĻČŌŚŃĪĖįÖŠ¼ÓČėµČĢå»żµÄĻĀĮŠČÜŅŗŅŌ¼õĀż·“Ó¦ĖŁĀŹµ«²»Ó°ĻģÉś³ÉĒāĘųµÄĮ攣ÄćČĻĪŖæÉŠŠµÄŹĒ____________(Ģī×ÖÄøŠņŗÅ)”£
A£®KClČÜŅŗ B£®ÅØŃĪĖį C£®ÕōĮóĖ® D£®CuSO4ČÜŅŗ
(2)ČēĶ¼ĪŖŌµē³Ų×°ÖĆŹ¾ŅāĶ¼£ŗ

¢Ł½«ĀĮʬŗĶĶʬÓƵ¼ĻßĻąĮ¬£¬Ņ»×é²åČėÅØĻõĖįÖŠ£¬Ņ»×é²åČėÉÕ¼īČÜŅŗÖŠ£¬·Ö±šŠĪ³ÉĮĖŌµē³Ų£¬ŌŚÕāĮ½øöŌµē³ŲÖŠ£¬×÷øŗ¼«µÄ·Ö±šŹĒ_______(Ģī×ÖÄø)”£
A£®ĀĮʬ”¢Ķʬ B£®Ķʬ”¢ĀĮʬ
C£®ĀĮʬ”¢ĀĮʬ D£®Ķʬ”¢Ķʬ
Š“³ö²åČėÅØĻõĖįČÜŅŗÖŠŠĪ³ÉµÄŌµē³ŲµÄøŗ¼«·“Ó¦Ź½£ŗ_______________”£
¢ŚČōAĪŖCu£¬BĪŖŹÆÄ«£¬µē½āÖŹĪŖFeCl3ČÜŅŗ£¬¹¤×÷Ź±µÄ×Ü·“Ó¦ĪŖ2FeCl3+Cu=2FeCl2+CuCl2”£Š“³öBµē¼«·“Ó¦Ź½£ŗ________£»øƵē³ŲŌŚ¹¤×÷Ź±£¬Aµē¼«µÄÖŹĮ潫_____(Ģī”°Ōö¼Ó”±”°¼õŠ””±»ņ”°²»±ä”±)”£ČōøƵē³Ų·“Ó¦ĻūŗÄĮĖ0.1mol FeCl3£¬Ōņ×ŖŅʵē×ӵďżÄæĪŖ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬ĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
A. ŗ¬ÓŠ“óĮæNO3£µÄČÜŅŗ£ŗH+”¢NH4+”¢I-”¢S2O32-
B. ÖŠŠŌČÜŅŗ£ŗFe3+”¢Al3+”¢NO3-”¢SO42-
C. ![]() =1”Į10-12µÄČÜŅŗ£ŗK+”¢AlO2-”¢CO32-”¢Na+
=1”Į10-12µÄČÜŅŗ£ŗK+”¢AlO2-”¢CO32-”¢Na+
D. ÓÉĖ®µēĄė³öµÄc(H+)=10-12mol/LµÄČÜŅŗ£ŗNa+”¢K+”¢CO32-”¢SO42-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ300 mLAl2(SO4)3ČÜŅŗÖŠ£¬ŗ¬Al3+1.62 g£¬ŌŚøĆČÜŅŗÖŠ¼ÓČė0.1molL©1Ba(OH)2ČÜŅŗ100mL£¬·“Ó¦ŗóČÜŅŗÖŠSO42-µÄĪļÖŹµÄĮæÅضČŌ¼ĪŖ( )
A. 0.4molL©1B. 0.3molL©1C. 0.2molL©1D. 0.1molL©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖN2+3H2![]() 2NH3ĪŖ·ÅČČ·“Ó¦£¬¶ŌøĆ·“Ó¦µÄĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
2NH3ĪŖ·ÅČČ·“Ó¦£¬¶ŌøĆ·“Ó¦µÄĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A.N2µÄÄÜĮæŅ»¶ØøßÓŚNH3
B.H2µÄÄÜĮæŅ»¶ØøßÓŚNH3
C.N2ŗĶH2µÄ×ÜÄÜĮæŅ»¶ØøßÓŚNH3µÄ×ÜÄÜĮæ
D.ŅņøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬¹Ź²»±Ų¼ÓČČ¾ĶæÉ·¢Éś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æFritz HaberŌŚŗĻ³É°±ĮģÓņµÄ¹±Ļ×¾ą½ńŅŃ¾110ÖÜÄź£¬µŖ×åŌŖĖŲ¼°Ęä»ÆŗĻĪļÓ¦ÓĆ¹ć·ŗ”£
(1)ŌŚ»łĢ¬13NŌ×ÓÖŠ£¬ŗĖĶā“ęŌŚ__________¶Ō×ŌŠżĻą·“µÄµē×Ó£¬ŗĖĶāµē×ÓÕ¼¾ŻµÄ×īøßÄܼ¶µÄµē×ÓŌĘĀÖĄŖĶ¼ĪŖ__________ŠĪ”£
(2)øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ£¬NH3”¢NO3-”¢NO2-ÖŠ£¬ÖŠŠÄŌ×Ó¼Ū²ćµē×Ó¶ŌŹż²»Ķ¬ÓŚĘäĖūĮ½ÖÖĮ£×ӵďĒ________£¬ÓėNO3-»„ĪŖµČµē×ÓĢåµÄ·Ö×ÓĪŖ__________”£Ņŗ°±ÖŠ“ęŌŚµēĄėĘ½ŗā2NH3![]() NH4+£«NH2-£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ£¬æÉĶĘÖŖNH2-µÄæռ乹ŠĶĪŖ__________£¬Ņŗ°±ĢåĻµÄŚ£¬µŖŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ________”£NH3±ČPH3øüČŻŅ×Ņŗ»ÆµÄŌŅņĪŖ__________________”£
NH4+£«NH2-£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ£¬æÉĶĘÖŖNH2-µÄæռ乹ŠĶĪŖ__________£¬Ņŗ°±ĢåĻµÄŚ£¬µŖŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ________”£NH3±ČPH3øüČŻŅ×Ņŗ»ÆµÄŌŅņĪŖ__________________”£
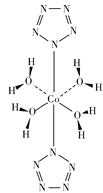
(3)ĪŅ¹śæĘѧ¹¤×÷ÕߏµĻÖŹĄ½ēŹ×“ĪČ«µŖŅõĄė×Ó(N5-)½šŹōŃĪCo(N5)2(H2O)4”¤4H2OµÄŗĻ³É£¬Ęä½į¹¹ČēĶ¼ĖłŹ¾£¬æÉÖŖN5-µÄ»Æѧ¼üĄąŠĶÓŠ______________”£
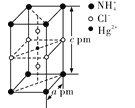
(4)°ŃĢŲ¶ØĪļÖŹµÄĮæÖ®±ČµÄNH4ClŗĶHgCl2ŌŚĆÜ·ā¹ÜÖŠŅ»Ęš¼ÓČČŹ±£¬Éś³É¾§ĢåX£¬Ę侧°ūµÄ½į¹¹Ķ¼¼°¾§°ū²ĪŹżČēĶ¼ĖłŹ¾”£Ōņ¾§ĢåXµÄ»ÆѧŹ½ĪŖ__________£¬Ę侧ĢåĆܶČĪŖ__________(Éč°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµĪŖNA£¬ĮŠ³ö¼ĘĖćŹ½)g”¤cm£3”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com