
| A. | Na2CO3 | B. | Na2O2 Na2CO3 | ||
| C. | NaOH Na2CO3 | D. | Na2O2 NaOH Na2CO3 |
分析 由2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,可知2mol碳酸氢钠分解生成1moNa2CO3、1molCO2、1molH2O,然后过氧化钠分别与水和二氧化碳反应,确定最后的固体的物质,据此进行解答.
解答 解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
2mol 1mol 1mol 1mol
2Na2O2+2CO2═2Na2CO3+O2,
1mol 1mol 1mol
则过氧化钠恰好与碳酸氢钠分解生成的二氧化碳反应,排出气体物质后冷却,最终残留的固体物质为2molNa2CO3,
故选A.
点评 本题考查化学方程式计算、钠的化合物的重要性质,题目难度不大,明确碳酸氢钠的性质及过氧化钠与二氧化碳、与水的反应及反应的先后顺序是解答本题的关键,试题培养了学生的化学计算能力.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:解答题
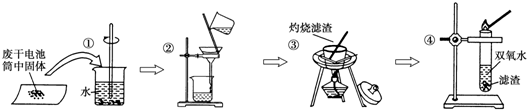
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
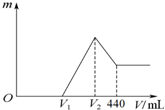
| A. | V2=400mL | |
| B. | 0≤V1<280mL | |
| C. | 加入NaOH溶液的过程中,产生沉淀的最大量可能为0.18mol | |
| D. | 当V1=160mL时,n(Mg)=0.04mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
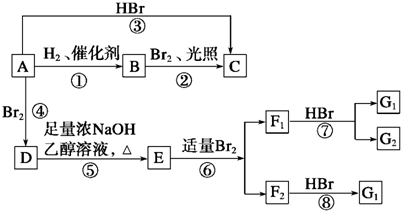
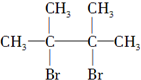 .
.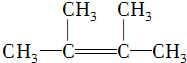 ,其名称为2,3-二甲基-2-丁烯.
,其名称为2,3-二甲基-2-丁烯. .
.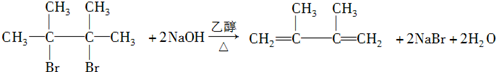 ;写出由E→F2的化学方程式
;写出由E→F2的化学方程式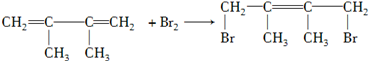 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COO-)+c(OH-)=0.10 mol•L-1 | B. | c(CH3COOH)+c(CH3COO-)=0.20 mol•L-1 | ||
| C. | c(CH3COOH)<c(CH3COO-) | D. | 温度为298 K时,pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.5 mol•L-1 Na2CO3溶液中含有的CO32-数目为0.5NA | |
| B. | 标准状况下,2.24 L C4H8含有的共用电子对数等于1.1NA | |
| C. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| D. | 27 g Al在标准状况下2.4 L Cl2中燃烧,转的2移的电子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
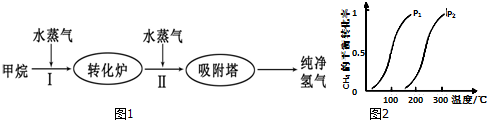
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com