
【题目】黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)下列基态原子或离子的价层电子排布图正确的_____________。
A ![]() B
B ![]()
C ![]() D
D ![]()
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的键角比水分子的______(填“大”或“小”)。
②X的沸点比水低的主要原因是___________。
(3)CuFeS2晶胞结构如图所示。
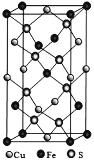
①Cu2+的配位数为__________,S2-的配位数为____________。
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏加德罗常数的值,CuFeS2晶体的密度是_______gcm-3(列出计算式)。
【答案】CD 小 水分子间存在氢键 4 4 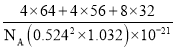
【解析】
根据核外电子排布规律判断价层电子排布图正误,利用电负性大小比较孤对电子斥力从而判断键角大小,根据均摊法及立体几何知识判断离子配位数并进行晶胞的相关计算。
(1)A.Fe2+的电子排布式为[Ar]3d6,价层电子排布图为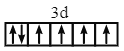 ,A错误;
,A错误;
B.Cu的电子排布式为[Ar]3d104s1,价层电子排布图为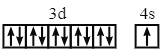 ,B错误;
,B错误;
C.Fe3+的电子排布式为[Ar]3d5,价层电子排布图为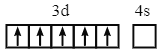 ,C正确;
,C正确;
D.Cu+的电子排布式为[Ar]3d10,价层电子排布图为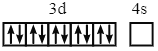 ,D正确;
,D正确;
故合理选项是CD;
(2)臭鸡蛋气味的气体X为H2S;
①因为O的电负性比S大而原子半径小于S,O—H键长要小一些,且O—H键上的电子更靠近O,斥力更大一些所以H2O键角要大于H2S;
②H2O分子间存在氢键,增加了分子之间的吸引作用,而H2S分子之间只存在分子间作用力,因此H2S的沸点比水低,故答案为:水分子间存在氢键;
(3)①晶胞结构分析可知,由面心上Cu2+与2个S2-相连,晶胞中每个Cu2+原子与4个S2-相连,则Cu2+的配位数为4;S2-与2个Fe2+和2个Cu2+相连,S2-的配位数为4;
②根据题给晶胞图可知,晶胞中Fe2+数目为:8×![]() +4×
+4×![]() +1=4,Cu2+的数目为:6×
+1=4,Cu2+的数目为:6×![]() +4×
+4×![]() =4,S2-数目为8,晶胞内共含4个CuFeS2,a=b=0.524nm,c=1.032nm,则晶体的密度ρ=
=4,S2-数目为8,晶胞内共含4个CuFeS2,a=b=0.524nm,c=1.032nm,则晶体的密度ρ=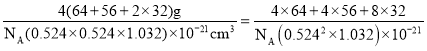 g/cm3,故答案为:4;4;
g/cm3,故答案为:4;4;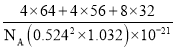 。
。


科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的的是( )
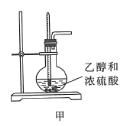
A.装置甲可用于实验室制备乙烯
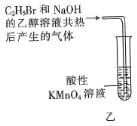
B.操作乙可用于检验![]() 与
与![]() 的乙醇溶液反应生成的气体中含有乙烯
的乙醇溶液反应生成的气体中含有乙烯
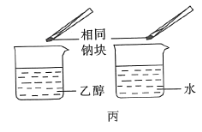
C.操作丙可用于比较乙醇中羟基的氢原子和水分子中氢原子的活泼性
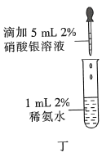
D.操作丁可用于配制银氨溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nsnnpn |
B | 基态原子中的未成对电子数是同周期中最多的 |
C | 原子最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)E元素在周期表中的位置是_________________________。
(2)写出D元素基态原子的简化电子排布式:__________。
(3)这5种元素中电负性最大的元素是__________(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为_______________________(填元素符号)。
(4)B、C、D的简单离子的半径由大到小的顺序为____________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次从左至右发生的反应类型和反应条件都正确的是 ( )
选项 | 反应类型 | 反应条件 |
A | 加成反应;取代反应;消去反应 | KOH醇溶液 |
B | 消去反应;加成反应;取代反应 | NaOH水溶液 |
C | 氧化反应;取代反应;消去反应 | 加热;KOH醇溶液 |
D | 消去反应;加成反应;水解反应 | NaOH醇溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铅-铜电池是一种电解质可循环流动的新型电池(如图所示),电池总反应为![]()
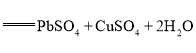 。下列有关该电池的说法正确的是( )
。下列有关该电池的说法正确的是( )
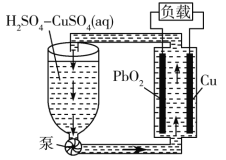
A.电池工作时,电子由Cu电极经电解质溶液流向PbO2电极
B.电池工作过程中,电解质溶液的质量逐渐减小
C.正极反应式:
D.电池工作过程中,两个电极的质量均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】来自植物精油中的三种活性成分的结构简式如下。下列说法正确的是
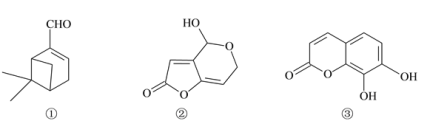
A.①中含有2个手性碳原子数
B.②难溶于水,分子中含有3种官能团
C.1 mol②、③与浓溴水反应,最多消耗2 mol Br2
D.1 mol③最多可与3 mol NaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】布洛芬具有降温和抑制肺部炎症的双重作用。一种制备布洛芬的合成路线如图:
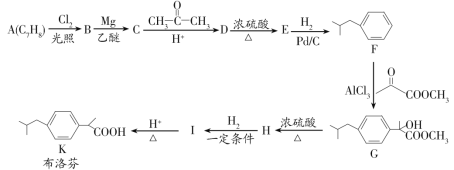
已知:①CH3CH2Cl![]() CH3CH2MgCl
CH3CH2MgCl
②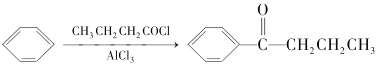 +HCl
+HCl
回答下列问题:
(1)A的化学名称为___,G→H的反应类型为___,H中官能团的名称为__。
(2)分子中所有碳原子可能在同一个平面上的E的结构简式为__。
(3)I→K的化学方程式为___。
(4)写出符合下列条件的D的同分异构体的结构简式__(不考虑立体异构)。
①能与FeCl3溶液发生显色反应;②分子中有一个手性碳原子;③核磁共振氢谱有七组峰。
(5)写出以间二甲苯、CH3COCl和(CH3)2CHMgCl为原料制备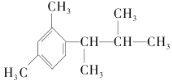 的合成路线:__(无机试剂任选)。
的合成路线:__(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下一定能大量共存的是
A.强酸性溶液中:H+、NO![]() 、SO
、SO![]()
B.pH=12的溶液中:OH-、K+、Cl-、HCO![]()
C.加入铝粉能放出氢气的溶液中一定存在:NH![]() 、NO
、NO![]() 、AlO
、AlO![]() 、SO
、SO![]()
D.25C时pH=7的无色溶液中:Na+、Cl-、SO![]() 、K+
、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用与反应原理设计不一致的是( )
A.热的纯碱溶液清洗油污:CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH-
+OH-
B.明矾净水:Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
C.用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量) ![]() TiO2xH2O↓+4HCl
TiO2xH2O↓+4HCl
D.配制氯化亚锡溶液时加入氢氧化钠:SnCl2+H2O![]() Sn(OH)Cl+HCl
Sn(OH)Cl+HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com