
����Ŀ����1����ѧ������ѧϰ��ѧ����Ҫ���ߡ��밴Ҫ���û�ѧ������գ�
��2��ͭԭ��___________��
��5������������______________��
����������Դ�����嵥��_________________��
������������Ԫ�صĻ��ϼ�Ϊ+3��________��
���������˹�����ĸɱ�______________��
��2��������л�ѧ������ϵѧ���Ļ�ѧ֪ʶ���ش��������⣺
�������ӵ�ʳ������ۡ��²ݡ����⡢ֲ���͡�ʳ�εȡ����и����������_________��
������ȱ____Ԫ���ܵ��¶�ͯ�������������Ͳ��������˻ᵼ�¹������ɡ�
������ϴ�Ӽ���ˮ�ܳ�ȥ�·��ϵ����ۣ���������ϴ�Ӽ���__________���á�
�����������������Ҫԭ������������е�________��ˮ���������˻�ѧ��Ӧ��
���������������衢����ֲ;ߵ��������г���������Ʒ�����������л��ϳɲ����Ƴɵ���____________.
���𰸡�2Cu5OH-H2![]() CO2��۸ƣ�����Ca�����黯����������O2����������
CO2��۸ƣ�����Ca�����黯����������O2����������
��������
��1����ԭ�ӵı�ʾ��������Ԫ�ط�������ʾһ��ԭ�ӣ���ʾ�����ԭ�ӣ�������Ԫ�ط���ǰ������Ӧ�����֡������ӵı�ʾ�������ڱ�ʾ�����ӵ�Ԫ�ط������Ͻǣ���������������������������������ǰ�����������ں�1�����ʱ��1Ҫʡ�ԡ�����ʾ��������ӣ����������ӷ���ǰ������Ӧ�����֡�����������Դ�����嵥���������������ϼ۵ı�ʾ�������ڸ�Ԫ�ص��Ϸ��������ź����ֱ�ʾ����������ǰ�������ں����ɱ��ǹ�̬�Ķ�����̼��
��2��������������������Ӫ���ص����ࡢʳ����Դ���з�����ɡ������ݸƵ��������ܺ�ȱ��֢���з������������ϴ�Ӽ������黯���ã����з�����������ڿ�������ʴ��ʵ���������������е�������ˮ��ͬ���õĽ�������л��ϳɲ��ϼ�ƺϳɲ��ϣ�Ҫ�ж��Ƿ����ںϳɲ��ϣ���ץס�����������л���ϳɸ߷��ӻ����
��1����ԭ�ӵı�ʾ��������Ԫ�ط�������ʾһ��ԭ�ӣ���ʾ�����ԭ�ӣ�������Ԫ�ط���ǰ������Ӧ�����֣���2��ͭԭ�ӱ�ʾΪ��2Cu�������ӵı�ʾ�������ڱ�ʾ�����ӵ�Ԫ�ط������Ͻǣ���������������������������������ǰ�����������ں�1�����ʱ��1Ҫʡ�ԡ�����ʾ��������ӣ����������ӷ���ǰ������Ӧ�����֣���5�����������ӿɱ�ʾΪ��5OH��������������Դ�����嵥�����������仯ѧʽΪ��H2�������ϼ۵ı�ʾ�������ڸ�Ԫ�ص��Ϸ��������ź����ֱ�ʾ����������ǰ�������ں�����������Ԫ�صĻ��ϼ�Ϊ+3�ۿɱ�ʾΪ��![]() ;���ɱ��ǹ�̬�Ķ�����̼���仯ѧʽΪ��CO2��
;���ɱ��ǹ�̬�Ķ�����̼���仯ѧʽΪ��CO2��
��2��������и������ۣ������������ࡣ������Ҫ�����ڹǸ�������У�ʹ�Ǻ����ݾ��м�Ӳ�Ľṹ֧�ܣ���ȱ����Ԫ��������������Ỽ���Ͳ��������˻Ỽ�������ɡ�������ϴ�Ӽ���ˮ�ܳ�ȥ�·��ϵ����ۣ�����Ϊϴ�Ӽ������黯���ã���ʹֲ���ͷ�ɢ������ϸС��Һ�Σ������۳ɴ�����顣�����������������Ҫԭ������������е�������ˮ�����˻�ѧ��Ӧ�������������������Ƴɵģ��������������л��ϳɲ��ϡ����������ò����Ƴɵģ��������ǽ������ϣ�����ֲ;����ò�����Ƴɵģ����ڽ������ϡ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�ؼס��ҡ���������������Ԫ����Ԫ�����ڱ��е�λ������ͼ��ʾ����������ͬ������ԭ�Ӱ뾶��С��Ԫ�ء������й��ж���ȷ����(����)
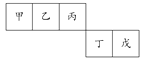
A. ��������������>��>��>��>��
B. �����ӵ����Ӱ뾶����>��
C. ���ж�Ԫ�ص����ж���
D. �ҵ��⻯����ֶ�����������������⻯�����һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʱ����ɫ������������ζ����˵���� ��
A. ����ֻ���е��� B. ������ֻ������
C. ����ʱ���Ǿۺϳɵ��� D. ����ʱ���۷�����ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�ס����������ʣ��������ᾧˮ�����ܽ�����ߣ�����˵����ȷ���ǣ� ��

A. �����ʵ��ܽ�ȴ��������ʵ��ܽ��
B. ���к����������ң������������ܼ��ķ����ᴿ��
C. t2��ʱ���ұ�����Һ�����ʵ���������һ��С�ڼױ����� Һ�����ʵ���������
D. t2��ʱ�����ס����������ʵ���Һ�ֱ�����t1�������������������һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ���칹�����
����ͬ�ķ��ӽṹ
����ͬ����Է�������
����ͬ�ķ���ʽ
����ͬ�����ʽ
����ͬ����������
A.�٢ڢ�B.�ڢۢ�
C.�٢ۢ�D.�ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ���Ϻ�ɫ�����ֳ���ͭ����ͭ�ĺϽ��л�ͭ����ͭ�Ͱ�ͭ�ȡ�����Cu��Zn�ĺϽ�ƻ�ͭ����ͭ�������ĵ����Ժ���ʴ�ԣ��������������������Ϊ�˲ⶨij��ͭ��Ʒ��ͭ������������ȡ20�˸û�ͭ��Ʒ���뵽50��ϡ�����У�ǡ����ȫ��Ӧ����������0.2������������
��1���û�ͭ��Ʒ��ͭ����������_________��
��2��ԭϡ������Һ��������������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ�ҳɹ��ϳ������������嵪��������(N5)6(H3O)3(NH4)4Cl(��R ����)���ش���������:
(1)��̬N ԭ���У��������ռ�ݵ�����ܲ�ķ�����______________��ռ�ݸ��ܲ���ӵĵ���������ͼ��״Ϊ_______________________________��
(2)N ��O ����Ԫ�ص�һ�����ܴ�С��ϵ��N__________( � >���� <�� �� =�� )O����ԭ����____________��N ��O����Ԫ�ص縺�Դ�С��ϵ��N_______(� >���� <�� ��=�� )O��
(3)��X-���������û�����R �ľ���ṹ����ֲ��ṹ����ͼ��ʾ��

����ɻ�����R �������������ЦҼ��ĸ���֮��Ϊ_________�������ĺ������ӵ����幹��Ϊ___________��������ԭ�ӵ��ӻ����������_______________________��
�ڷ����еĴ�м����÷���![]() ��ʾ������m ���������γɵĴ�м�ԭ������n ���������γɵĴ�м����������籽�����еĴ�м��ɱ�ʾΪ
��ʾ������m ���������γɵĴ�м�ԭ������n ���������γɵĴ�м����������籽�����еĴ�м��ɱ�ʾΪ![]() ����N5-�еĴ�м�Ӧ��ʾΪ___________________��
����N5-�еĴ�м�Ӧ��ʾΪ___________________��
�����ͨ����X-H��������Y ��ʾ�����ʾ����ͼ�е���������:_________________��
��R��������������Ϊa nm�������к���Y��(N5)6(H3O)3(NH4)4Cl ��Ԫ�����(N5)6(H3O)3(NH4)4Cl����Է���������M ��ʾ�������ӵ�������ֵΪNA����R ������ܶ�Ϊ________g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����͵⡢������ػ������ڻ��������ϵ��������Ź㷺��Ӧ�á��ش��������⣺
(1)��̬Feԭ���У�����δ�ɶԵ�����Ϊ________�������ĵ���������I3(Fe)���̵ĵ��������I3(Mn)С��ԭ����__________________________________________________��
(2)NaNO2����������ʳƷ�ķ�ɫ����������NO2-�ļ��ι���Ϊ_________������ԭ�ӵ��ӻ��������Ϊ_________��
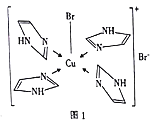
(3)Cu2+��һ�������ķ��ӽṹ��ͼ1��ʾ����λԭ��Ϊ________������![]() �����ЦҼ�����Ϊ________���������еĴ�м����÷���
�����ЦҼ�����Ϊ________���������еĴ�м����÷���![]() ��ʾ,����m���������γɴ�м���ԭ������n���������γɴ�м��ĵ�����(�籽�����еĴ�м��ɱ�ʾΪ
��ʾ,����m���������γɴ�м���ԭ������n���������γɴ�м��ĵ�����(�籽�����еĴ�м��ɱ�ʾΪ![]() ),��
),��![]() �еĴ�м�Ӧ��ʾΪ________________��
�еĴ�м�Ӧ��ʾΪ________________��

(4)һ�������������ɲ�ͬ��̬����ԭ��[Fe(A)��Fe(B)]����ԭ�ӹ���,�侧���ڲ���ͼʾ�����ֽṹ,�����IJ��ֽṹ��ͼ2��
�ٸ�����������Ļ�ѧʽΪ_________,���۵�Ϊ1594.5 ��,��������_________ (�ԭ�ӡ������ӡ����ӡ�)���塣
�ڸþ����߳�Ϊa pm,�����ܶ�Ϊ____________________g��cm-3(�г�����ʽ����)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com