
ÓĆĆ«±ŹÕŗȔɣĮæ30% FeCl3ČÜŅŗŌŚĶʬÉĻŠ“Ņ»øö”°Cu”±×Ö,·ÅÖĆʬæĢ,ÓĆÉŁĮæĖ®½«ĶʬÉĻµÄČÜŅŗ³åµ½Š”ÉÕ±ÖŠ,ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A.ÉÕ±ÖŠµÄČÜŅŗ³Ź»ĘÉ«
B.ĶʬĪŽČĪŗĪ±ä»Æ
C.ĶʬÉĻÓŠ°¼ĻŻµÄ”°Cu”±×Ö
D.·¢ÉśĮĖ·“Ó¦:Fe3++Cu====Cu2++Fe2+
 ÓŵČÉśĢāæāĻµĮŠ“š°ø
ÓŵČÉśĢāæāĻµĮŠ“š°ø 53ĢģĢģĮ·ĻµĮŠ“š°ø
53ĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ
A£®NaOHČÜŅŗæɱ£“ęŌŚÅä²£Į§ČūµÄŹŌ¼ĮĘæÖŠ
B£®NaŌŚæÕĘųÖŠ³¤ĘŚ·ÅÖĆ£¬×īÖÕ±äĪŖNaHCO3·ŪÄ©
C£®¶žŃõ»ÆĮņ¾ßÓŠ½ĻĒæµÄ»¹ŌŠŌ£¬¹Ź²»ÄÜÓĆÅØĮņĖįøÉŌļ
D£®ÅØĻõĖįŌŚ¹āÕÕĢõ¼žĻĀ“ę·ÅŅ×±ä»Ę£¬ŹĒŅņĪŖĻõĖį·Ö½āÉś³ÉµÄNO2ČÜÓŚÅØĻõĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓėĖ÷¶ūĪ¬ÖĘ¼ī·ØĻą±Č£¬ŗīµĀ°ńÖĘ¼ī·Ø×īĶ»³öµÄÓŵćŹĒ
A£®ŌĮĻĄūÓĆĀŹøß B£®Éč±øÉŁ
C£®Ń»·ĄūÓƵÄĪļÖŹ¶ą D£®ŌĮĻŅ×µĆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆŗ¬ÉŁĮæĆ¾·ŪµÄĀĮ·ŪÖĘČ”“æ¾»µÄĒāŃõ»ÆĀĮ,ĻĀŹö²Ł×÷²½ÖčÖŠ×īĒ”µ±µÄ×éŗĻŹĒ””
(””””)
¢Ł¼ÓŃĪĖįČܽā””¢Ś¼ÓÉÕ¼īČÜŅŗČܽā””¢Ū¹żĀĖ””¢ÜĶØČė¹żĮæCO2Éś³ÉAl(OH)3³Įµķ””¢Ż¼ÓČėŃĪĖįÉś³ÉAl(OH)3³Įµķ””¢Ž¼ÓČė¹żĮæÉÕ¼īČÜŅŗ
A.¢Ł¢Ž¢Ż¢Ū”” B.¢Ś¢Ū¢Ü¢Ū”” C.¢Ś¢Ū¢Ż¢Ū”” D.¢Ł¢Ū¢Ż¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĀČ»ÆĪļÖŠ,¼ČÄÜÓɵ„ÖŹÖ±½Ó»ÆŗĻÖʵĆ,ÓÖæÉÓɽšŹōŗĶŃĪĖį·“Ó¦ÖʵƵďĒ(””””)
A.CuCl2 B.FeCl2
C.FeCl3 D.AlCl3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĮņĖįŃĒĢś¾§Ģå(FeSO4”¤7H2O)ŌŚŅ½Ņ©ÉĻ×÷²¹ŃŖ¼Į”£Ä³æĪĶāŠ”×éµÄĶ¬Ń§Óū²ā¶ØøĆ²¹ŃŖ¼ĮÖŠĢśŌŖĖŲµÄŗ¬Į攣ŹµŃé²½ÖčČēĻĀ:
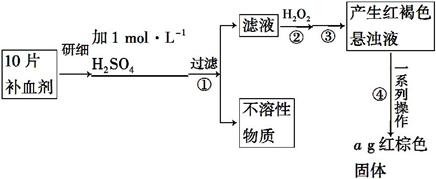
Ēė»Ų“šĻĀĮŠĪŹĢā:
(1)Ö¤Ć÷²½Öč¢ŁĀĖŅŗÖŠŗ¬ÓŠFe2+µÄ·½·ØŹĒ:Ȕѳ,ĻȵĪ¼ÓKSCNČÜŅŗ,ŌŁµĪ¼Ó””””””””,øĆ¹ż³ĢµÄĻÖĻóĪŖ__________________________________________”£
(2)²½Öč¢Ś¼ÓČė¹żĮæH2O2µÄÄæµÄŹĒ _____________________________________”£
(3)²½Öč¢ŪÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ _____________________________________”£
(4)²½Öč¢ÜÖŠŅ»ĻµĮŠ“¦ĄķµÄ²Ł×÷²½Öč:¹żĀĖ”¢________”””¢×ĘÉÕ”¢”””””””””¢³ĘĮ攣
(5)ČōŹµŃéÖŠĢśĪŽĖšŗÄ,ŌņĆæʬ²¹ŃŖ¼ĮÖŠŗ¬ĢśŌŖĖŲµÄÖŹĮæĪŖ””””””””g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ć¾Ņ»¹żŃõ»ÆĒāČ¼ĮĻµē³Ų¾ßÓŠ±ČÄÜĮæøß”¢°²
Č«·½±ćµČÓÅµć£¬Ęä×Ü·“Ó¦ĪŖMg+H2O2+H2SO4 MgSO4+2H2O£¬½į¹¹Ź¾ŅāĶ¼ČēĶ¼ĖłŹ¾”£ĻĀĮŠ¹ŲÓŚøƵē³Ų µÄ
µÄ
ŠšŹöÕżČ·µÄŹĒ
A£®µē³ŲÄŚ²ææÉŅŌŹ¹ÓĆMnO2×÷ĢīĮĻ
B£®µē³Ų¹¤×÷Ź±£¬H+ĻņMgµē¼«ŅʶÆ
C£®µē³Ų¹¤×÷Ź±£¬Õż¼«µÄµē°å·“Ó¦Ź½ĪŖMg—2e— Mg2+
D£®µē³Ų¹¤×÷Ź±£¬µē½āÖŹČÜŅŗµÄpH½«²»¶Ļ±ä“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÉĻŗ£ŹĄ²©»įĘŚ¼ä£¬ŌŚµĀ¹ś¹ŻµÄŗŗ±¤Ö®¼ŅÕ¹¹ŻČĖĆĒ擵½Ņ»øö1”Ć20·É»śČ¼ĮĻµē³ŲµÄÄ£ŠĶ”£Č¼ĮĻµē³ŲŹĒŅ»
ÖÖĶعżĒāŃõ½įŗĻĄ“·¢µēµÄµē»ÆѧװÖĆ”£Ä³ĒāŃõČ¼ĮĻµē³ŲµÄµē³Ų·“Ó¦ĪŖ2H2£«O2===2H2O£¬µē½āŅŗĪŖKOHČÜ
Ņŗ”£ĒāŃõČ¼ĮĻµē³ŲµÄĶ»³öÓŵćŹĒ°Ń________ÄÜÖ±½Ó×Ŗ»ÆĪŖ________ÄÜ£¬¶ų²»ÓĆ¾¹ż________ÄÜÕāŅ»ÖŠ¼äŠĪ
Ź½”£
 £Ø1£©ÓŠ¹ŲĒāŃõČ¼ĮĻµē³ŲµÄĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ (””””)
£Ø1£©ÓŠ¹ŲĒāŃõČ¼ĮĻµē³ŲµÄĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ (””””)
A£®“Ėµē³ŲÄÜ·¢³öĄ¶É«»šŃę
B£®ĒāĘųĪŖÕż¼«£¬ŃõĘųĪŖøŗ¼«
C£®ŅņĪŖÉś³ÉĖ®£¬ĖłŅŌ¹¤×÷Ź±ČÜŅŗµÄ¼īŠŌŌ½Ą“Ō½Ēæ
D£®øŗ¼«ÉĻĒāĘųŹ§µē×Ó£¬·¢ÉśŃõ»Æ·“Ó¦£»Õż¼«ÉĻŃõĘųµĆµē×Ó£¬·¢Éś»¹Ō·“Ó¦
£Ø2£©øƵē³ŲĖł²śÉśµÄĖ®æÉŅŌ×÷ĪŖŅūÓĆĖ®£¬½ńÓūÖʵĆ ³£ĪĀĻĀ1 LĖ®£¬Ōņµē³ŲÄŚ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ________”£
³£ĪĀĻĀ1 LĖ®£¬Ōņµē³ŲÄŚ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ________”£
A£®8.9”Į10£3 mol B£®4.5”Į10£2 mol
C£®1.1”Į102 mol D£®5.6”Į103 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĀĮµē³ŲŠŌÄÜÓÅŌ½£¬AlAgOµē³ŲæÉÓĆ×÷Ė®ĻĀ¶ÆĮ¦µēŌ“£¬ĘäŌĄķČēĶ¼ĖłŹ¾”£øĆ
µē³Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________________________________”£
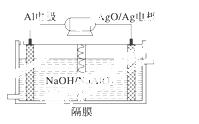
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com