
| A. | 简单离子半径:E<D | |
| B. | 气态氢化物的稳定性:B<E | |
| C. | 最高价氧化物对应水化物的碱性:C>D | |
| D. | A与E形成的化合物为离子化合物 |
分析 A、B、C、D、E五种短周期主族元素原子序数逐渐增大,其中A与C、B与E分别为同族元素.B原子最外层电子数是次外层的3倍,则B有2个电子层,最外层有6个电子,则B为氧元素,B与E分别为同族元素,则E为硫元素;原子半径A<B<E<D<C,则C、D与E为同周期元素,C、D的核外电子数之和与B、E核外电子数之和相等为24,所以C为钠元素,D为铝元素;A与C为同族元素,则A为氢元素.以此解答该题.
解答 解:A、B、C、D、E五种短周期主族元素原子序数逐渐增大,其中A与C、B与E分别为同族元素.B原子最外层电子数是次外层的3倍,则B有2个电子层,最外层有6个电子,则B为氧元素,B与E分别为同族元素,则E为硫元素;原子半径A<B<E<D<C,则C、D与E为同周期元素,C、D的核外电子数之和与B、E核外电子数之和相等为24,所以C为钠元素,D为铝元素;A与C为同族元素,则A为氢元素.
A.D为铝元素,E为硫元素,硫离子核外电子层比铝离子多,离子半径硫离子较大,即D<E,故A错误;
B.B为氧元素,E为硫元素,非金属性O>S,气态氢化物的稳定性B>E,故B错误;
C.C为钠元素,D为铝元素,金属性Na>Al,所以最高价氧化物对应水化物的碱性C>D,故C正确;
D.A为氢元素,E为硫元素,二者形成的化合物为H2S,为共价化合物,故D错误.
故选C.
点评 本题以元素推断为载体,考查原子结构与位置关系、元素化合物知识、元素周期律递变规律等,为高考常见题型,侧重于学生的分析能力的考查,难度中等,推断元素是解题关键,注意规律的掌握与运用.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Al3+、K+、SO42-、Cl-、Al[(OH)4]- | B. | Al3+、Na+、Cl-、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、NO3-、Cl- | D. | Fe2+、H+、Br-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液:CO32-+2H2O?H2CO3+2OH- | |
| B. | NH4Cl溶液:NH4++H2O?NH3•H2O+H+ | |
| C. | CuSO4溶液:Cu2++2H2O?Cu(OH)2↓+2H+ | |
| D. | NaClO溶液:ClO-+H2O═HClO+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试样 | 所加试剂 | 实验现象 |
| 第一份试液 | 滴加适量的淀粉KI溶液 | 呈蓝色 |
| 第二份试液 | 滴加用盐酸酸化的BaCl2溶液 | 有白色沉淀 |
| 第三份试液 | 滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体(n)的关系如右图 |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
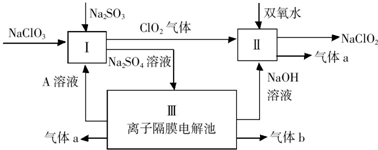
 ;Ⅰ中发生反应的还原剂是Na2SO3(填化学式).
;Ⅰ中发生反应的还原剂是Na2SO3(填化学式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | C、Al、P | D. | O、P、Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸可用于雕刻玻璃,说明氢氟酸具有强酸性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸具有强氧化性 | |
| C. | 常温下浓硫酸可用铝罐贮存,说明铝与浓硫酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨水显碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com