
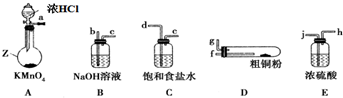

分析 I.实验室中以粗铜(含杂质Fe)为原料制备铜的氯化物,浓盐酸和高锰酸钾发生反应生成氯气,氯气中混有氯化氢和水,可用饱和食盐水除去氯化氢,用浓硫酸干燥,加热时硬质试管中铜和氯气反应生成氯化铜,用氢氧化钠溶液吸收氯气尾气,防止污染空气,
(1)仪器A为圆底烧瓶;
(2)KMnO4与浓盐酸制取的Cl2含有HCl和H2O,用饱和食盐水除去HCl,用浓硫酸除去H2O,然后Cl2与Cu反应,最后用NaOH溶液吸收未反应的Cl2,防止污染空气;
(3)利用止水夹夹住导气管的橡皮管,从长颈漏斗中加水至漏斗内外形成液面高度差,一段时间内,液面高度差不变,说明气密性良好;
(4)D中发生反应有:氯气与Cu反应生成氯化铜,与Fe反应生成氯化铁;
(5)装置B吸收未反应的氯气,反应生成NaCl、NaClO,NaClO具有漂白性,钢铁制品表面生成红褐色沉淀、溶液会失去漂白、杀菌消毒功效,说明ClO-在正极上得电子,发生还原反应生产Cl-,由于为碱性条件,还生成OH-;
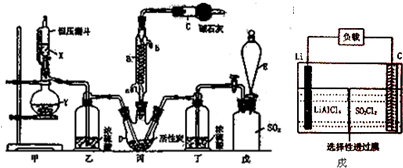
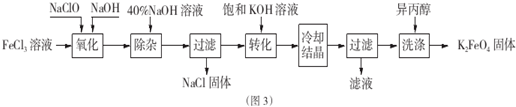
Ⅱ.粗铜(含杂质Fe)与氯气反应生成氯化铁和氯化铜,加稀盐酸溶解,形成氯化铁和氯化铜溶液,再加CuO或氢氧化铜等调节pH,使铁离子转化为氢氧化铁沉淀,过滤得到的固体为氢氧化铁,溶液2为氯化铜溶液,通入二氧化硫,二氧化硫与铜离子发生氧化还原反应生成CuCl,氯化铜溶液在HCl氛围中蒸发结晶得到CuCl2•2H2O;
(3)由2Cu2++4I-=2CuI↓+I2、I2+2S2O32-=S4O42-+2I-,可得关系式2n(ClCl2)~I2~2n(S2O32-),据此计算200mL溶液中n(ClCl2),进而计算ClCl2的质量分数.
解答 解:I.(1)根据装置图可知,装置A中仪器Z的名称为圆底烧瓶,
故答案为:圆底烧瓶;
(2)仪器连接顺序:Cl2发生装置→除去HCl气体装置→干燥装置→制备装置→多余Cl2处理装置,所以各仪器接口顺序是:a→d、e→j、h→f、g→b;该实验中有有毒气体参加反应,所以实验前要检验装置的气密性;
故答案为:d;e;j;h;f;g;b;
(3)检验装置A的气密性的方法是:用弹簧夹夹住a处橡皮管并关闭分液漏斗的活塞,向分液漏斗中加入较多的水,然后打开分液漏斗的活塞,使水缓缓流下,若分液漏斗中的水不能完全漏下,说明装置气密性好(或在a管处接一导管,并将导管末端插入水中,同时关闭分液漏斗的活塞,用酒精灯给圆底烧瓶微热,若导管末端有气泡冒出,且停止加热恢复室温时,导管末端形成一段小水柱,说明装置气密性好),
故答案为:用弹簧夹夹住a处橡皮管并关闭分液漏斗的活塞,向分液漏斗中加入较多的水,然后打开分液漏斗的活塞,使水缓缓流下,若分液漏斗中的水不能完全漏下,说明装置气密性好(或在a管处接一导管,并将导管末端插入水中,同时关闭分液漏斗的活塞,用酒精灯给圆底烧瓶微热,若导管末端有气泡冒出,且停止加热恢复室温时,导管末端形成一段小水柱,说明装置气密性好);
(4)硬质试管中发生反应有:氯气与Cu反应生成氯化铜,与Fe反应生成氯化铁,反应方程式分别为:Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2、2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3;
故答案为:Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2、2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3;
(5)根据题意,装置B中溶液含有次氯酸钠,有强氧化性,所以钢铁(含Fe、C)在该溶液中会被次氯酸根氧化,所以该电化学腐蚀过程中,次氯酸根作氧化剂在正极发生还原反应,正极反应式为ClO-+2e-+H2O═Cl-+2OH-,
故答案为:ClO-+2e-+H2O═Cl-+2OH-;
Ⅱ.(1)固体中主要是氯化铁和氯化铜,在水溶液中能水解,所以用稀盐酸溶解固体可以抑制其水解,
故答案为:抑制Cu2+、Fe3+水解;
(2)根据信息可知:在加热条件下,SO2与铜离子反应生成CuCl白色沉淀和SO42-,其反应的离子方程式为:2Cu2++2Cl-+SO2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+4H++SO42-;
故答案为:2Cu2++2Cl-+SO2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+4H++SO42-;
(3)由2Cu2++4I-=2CuI↓+I2、I2+2S2O32-=S4O42-+2I-,可得关系式2n(ClCl2)~I2~2n(S2O32-),故200mL溶液中n(ClCl2)=n(S2O32-)=0.02L×0.2mol/L×$\frac{200mL}{2mL}$=0.4mol,则样品中m(ClCl2)=0.4mol×135g/mol=54g,则ClCl2的质量分数为$\frac{54g}{65g}$×100%=83.1%,故答案为:83.1%.
点评 本题考查物质的制备实验方案、化学工艺流程,涉及对装置及操作的分析评价、气密性检验、电化学腐蚀、滴定计算等,侧重于基础知识的综合应用,难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、Al--电解质 | B. | C2H4、O2--易燃气体 | ||
| C. | CaC2、K--遇湿易燃物品 | D. | KMnO4、KClO3--还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
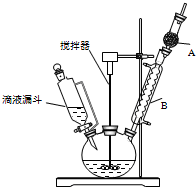 三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.| 物质 | 沸点/℃ |
| 三苯甲醇 | 380 |
| 乙醚 | 34.6 |
| 溴苯 | 156.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物总能量为679kj | |
| B. | 生成物总能量为431kj | |
| C. | 氢气和氯气反应生成2mol氯化氢气体,反应放出183kJ能量 | |
| D. | 氢气和氯气反应生成2mol氯化氢气体,反应吸收183kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的分子式:CH3CH2OH | B. | 次氯酸的电子式: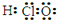 | ||
| C. | NH4Cl的电子式: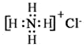 | D. | 乙醛结构简式:CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com