
| A. | 无色溶液:Ca2+、Na+、Cl-、HCO3- | |
| B. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | |
| C. | 水电离出的c(H+)=10-13mol•L-1的溶液中:K+、Na+、SO42-、AlO2- | |
| D. | 有较多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3- |
分析 A.该组离子之间不反应,且均为无色;
B.能使pH试纸呈红色的溶液,显酸性;
C.水电离出的c(H+)=10-13mol•L-1的溶液,为酸或强碱溶液;
D.离子之间结合生成络离子,离子之间发生水解反应.
解答 解:A.该组离子之间不反应,可大量共存,且均为无色,故A选;
B.能使pH试纸呈红色的溶液,显酸性,H+、I-、NO3-发生氧化还原反应,不能共存,故B不选;
C.水电离出的c(H+)=10-13mol•L-1的溶液,为酸或强碱溶液,酸溶液中不能大量存在AlO2-,故C不选;
D.Fe3+、SCN-结合生成络离子,Fe3+、HCO3-发生相互促进水解反应,不能共存,故D不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应、水解反应判断,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 过滤操作中,漏斗的尖端应接触烧杯内壁 | |
| B. | 用玻璃棒蘸取CH3COOH溶液点在水湿润的pH试纸上,测定该溶液的pH | |
| C. | 中和滴定时.滴定管用所盛装的反应液润洗2~3 次. | |
| D. | 分液操作中,下层液体从下端放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
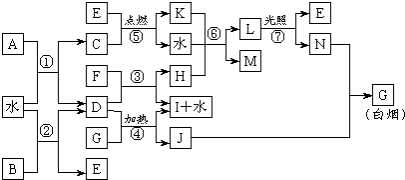
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质参加和单质生成的化学反应一定是氧化还原反应 | |
| B. | 盐酸是强酸,所以盐酸是强电解质 | |
| C. | 向FeCl3饱和溶液滴加NaOH溶液可制备Fe(OH)3胶体 | |
| D. | 化合反应不一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
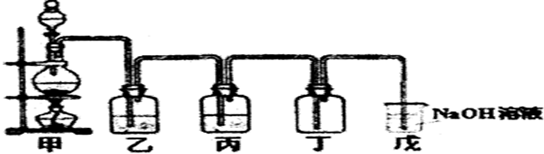
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
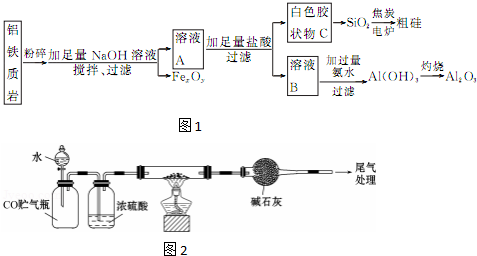
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.1g C12与足量NaOH溶液反应转移的电子数为0.2NA | |
| B. | 46 g NO2 和 N2O4混合气体中含有原子数为3NA | |
| C. | 1mol Na2O2 固体中含离子总数为4NA | |
| D. | 标准状况下,2.24L辛烷所含分子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com