
����Ŀ��������Ϊ���ӳ��ʻ���������ͨ�����ڻ�ƿ�м����ʻ����ʼ����±���0.5 Lij���ʻ����ʼ��к��еijɷּ��������Ķ���ش��������⣺
�ɷ� | ����(g) | Ħ������(g/mol) |
����(C12H22O11) | 25.00 | 342 |
�����(K2SO4) | 0.25 | 174 |
�������(KMnO4) | 0.25 | 158 |
��˾ƥ��(C9H8O4) | 0.17 | 180 |
������(AgNO3) | 0.02 | 170 |
(1)�ʻ����ʼ������гɷ��У����ڵ���ʵ���________(����ĸ)��
a������ b�������
c��������� d��������
(2)������480 mL���ʻ����ʼ��������ṩ����������
�ٽ�ͷ�ιܡ�����Ͳ�����ձ�����ҩ�ס��ݵ�����ƽ����Ҫ���ʵ�飬ȱ�ٵIJ�����������________(д��������)��
(3)д�����ʻ����ʼ���K�������ʵ���Ũ�ȵļ���ʽ��________(���ػ���)��
(4)��m g������ȫȼ�պ�IJ���ͨ��������Na2O2���壬��ַ�Ӧ�������ӵ�����________(����������������������)m g��
���𰸡�bcd����������500 mL����ƿ�� ![]() mol/L��
mol/L��
��������
(1)��������ˮ��Һ������״̬�¾�������Ļ�������ڷǵ���ʣ���a��������ء�������ء�������������ˮ��Һ������״̬�¶��ܵ���Ļ�������ڵ���ʣ���b��c��d��ȷ��
(2)����480 mLһ��Ũ�ȵ���Һʱ���õ��������е�����ƽ���ձ�������������ͷ�ιܡ�500 mL����ƿ�ȡ�
(3)K2SO4�����ʵ���Ϊ![]() mol��KMnO4�����ʵ���Ϊ
mol��KMnO4�����ʵ���Ϊ![]() mol������K�������ʵ���Ũ��Ϊ
mol������K�������ʵ���Ũ��Ϊ![]() mol/L��
mol/L��
(4)������ȫȼ������CO2��ˮ��Ȼ��ֱ�������Ʒ�Ӧ����2CO2��2Na2O2=2Na2CO3��O2��2H2O��2Na2O2=4NaOH��O2��������������Ӧ�У���Na2O2������ԣ�Na2O2���ص�����ʵ����H2O��H2��������CO2��CO���������������ɿ���Na2O2��H2=2NaOH��Na2O2��CO=Na2CO3�������ǵķ���ʽ�ɱ�ʾΪ(CO)11H22C����������ӵ������������ǵ�������


 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. ϡ��������м��Ӧ:2Fe+6H+=2Fe3++3H2��
B. ��NH4HCO3��Һ�мӹ�����NaOH��Һ������:NH4++OH-=NH3��+H2O
C. �����Ե⻯����Һ�еμ�������˫��ˮ:2I-+2H++H2O2=I2+2H2O
D. HS-�ĵ���:HS-+H2O![]() OH-+HS-
OH-+HS-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʣ����ܰ� ![]() (��������ʾ��Ӧһ�����)��ϵת�������� ��
(��������ʾ��Ӧһ�����)��ϵת�������� ��
ѡ�� | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | NaOH | NaHCO3 | Na2CO3 |
C | Al | Al(OH)3 | Al2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼʾ����һ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
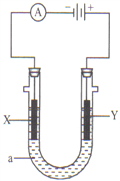
��X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ�� ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��Ӧʽ�ǣ�______________����X�������۲쵽�������ǣ�__________________��
��Y�缫�ϵĵ缫��Ӧʽ�ǣ�_____________________��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ�����_____��
��Y�缫�ĵ缫��Ӧʽ��_____________________�������������ʷ�Ӧ��
��3����Ҫ�����������ͭ��X�缫�IJ�����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.�����ЧӦ�����ڼ��������Һ
B.�������ӵ�ֱ����1��100 nm֮��
C.����һ���ǻ����
D.��FeCl3ϡ��Һ������ˮ�����Ƶ�Fe��OH��3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ̬���������ᣨ�е�118�棩�������������е�77.1�棩�������ͺ�ˮ����ˮ����ʵ���ҷ��������ֻ�������ȷ��������Ϊ�� ��
A.����Һ����ȡ
B.��ȡ������Һ
C.��Һ��������ȡ
D.������ȡ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��Aԭ�ӵ�L���Ӳ��Ԫ��Bԭ�ӵ�L���Ӳ��� 3�����ӣ�BԪ��ԭ�Ӻ������������AԪ��ԭ�Ӻ������������5������A��B�γɵĻ�����Ļ�ѧʽ����Ϊ(����)
A.B2A3B.B3A2
C.A2B3D.BA2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijǿ������ҺX�п��ܺ���Ba2+��Al3+��NH4+��Fe2+��Fe3+��CO32����SO32����SO42����Cl����NO3���е�һ�ֻ��֣�ȡ����Һ��������ʵ�飬ʵ��������£�

����������Ϣ���ش��������⣺
��1����������������ʵ�鲻��ȷ����ҺX���Ƿ��е����������ӷֱ��� ����֤�����������Ƿ���ڵļ�ʵ�����Ϊ____ __��
��2�������ӷ��̱������з�Ӧ��
������������A�� ������������ҺH�� ��
��3��������������������Ũ��Ϊ2mol/L��������l0mlʱ��ʼ����������55mlʱ���������ﵽ���ֵ0.03mol�������μӳ����������ֲ��䣬����ٵμӳ��������ܽ⣬��60mlʱ����������Ϊ0.025mol�ұ��ֲ��䣬��ԭ��Һ��c��Fe2+��Ϊ mol/L��c��Fe3+��Ϊ mol/L��c��Cl����Ϊ mol/L��������Щ���Ӳ����ڣ�����0mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ���⡣
(1)�õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��
___ C+ ___ KMnO4+ H2SO4 �� ____CO2��+ ____MnSO4 + ____K2SO4+
(2)����ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g)![]() CO2(g)��H2(g)���õ����¶������ݣ�
CO2(g)��H2(g)���õ����¶������ݣ�
ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
��ʵ��1����CO2��ʾ�Ļ�ѧ��Ӧ����Ϊ__________������С������λ������ͬ����
��ʵ��2������ƽ�ⳣ��K=_________���÷�ӦΪ _____��������š����ȷ�Ӧ��
(3)��֪�ڳ��³�ѹ�£�
�� 2CH3OH(l)��3O2(g) �� 2CO2(g)��4H2O(g) ��H �� ��1275.6 kJ��mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H �� ��566.0 kJ��mol
�� H2O(g) �� H2O(l) ��H �� ��44.0 kJ��mol
д���״�����ȫȼ������һ����̼����̬ˮ���Ȼ�ѧ����ʽ��_____________��
(4)ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ��ʾ�ĵ��װ�á�

�ٸõ�ظ����ĵ缫��ӦΪ��_______________��
�ڸõ�ع���ʱ����Һ�е�OH����______���ƶ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com