
Ⅰ.某兴趣小组用如图装置做了两次实验。
实验①:向甲池的Pt电极表面通氢气,发现电流计指针发生了偏转,乙池的Pt电极表面出现气泡。
实验②:向乙池的Pt电极表面通氧气,发现电流计指针也发生了偏转,且偏转方向与实验①相同,同时甲池的Pt电极表面也出现气泡。
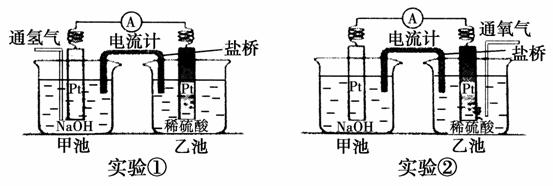
(1)实验①,甲池通氢气的Pt电极为________________极,电极反应式为_________________________________________________。
(2)实验②,乙池通氧气的Pt电极为________________极,电极反应式为__________________________________________________。
(3)两次实验中原电池的总反应相同,总反应的离子方程式为___
__________________________________________________________。

Ⅱ.电解法污水处理技术已很成熟。富含悬浮物的工业污水采用如图装置进行处理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,吸附部分悬浮物沉降,同时阴极产生的气泡将部分悬浮物带到水面形成浮渣层,然后滤去沉淀、撇掉浮渣层。富含有机废物的生活污水也可用同样方法进行处理。污水中的有机废物能被阳极的某一产物迅速降解成二氧化碳、水等无机物。
(1)在电解处理过程中,若污水中离子浓度较小,导电能力较差,处理效率下降,此时可向污水中加入适量的________。
a.BaSO4 b.CH3COOH
c.NaNO3 d.CH3OH
(2)电解处理过程中,阳极实际发生了两个电极反应,阳极的电极反应式分别是①________________;②________________。
解析:本题考查了电化学知识,意在考查考生对电化学知识综合运用的能力。Ⅰ.(1)实验①中,通氢气的一极为负极,在碱性条件下,电极反应方程式为H2+2OH--2e-===2H2O。(2)实验②中,通氧气的一极为正极,在酸性条件下,电极反应方程式为O2+4H++4e-===2H2O。(3)两次实验中原电池的总反应相同,总反应的离子方程式为:H++OH-===H2O。Ⅱ.(1)要增强溶液的导电能力,但不能使电极反应发生改变,故加入溶于水的强电解质,如题中的NaNO3,即选c。(2)电解过程中,铁为阳极,铁先失去电子,Fe-2e-===Fe2+,同时,还会发生:2H2O-4e-===4H++O2↑。
答案: Ⅰ.(1)负(1分) H2-2e-+2OH-===2H2O(1分) (2)正(1分) O2+4e-+4H+===2H2O(1分) (3)H++OH-===H2O(2分)
Ⅱ.(1)c(2分) (2)①Fe-2e-===Fe2+(1分)
②2H2O-4e-===O2↑+4H+(1分)


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
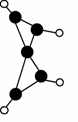
科学家最近在-100℃的低温下合成一种烃X,此分子的模型如右图
(图中的连线表示化学键),下列说法正确的是( )
A.X能使溴的四氯化碳溶液褪色
B.X是一种在常温下能稳定存在的液态烃
C.X分子中在同一平面上的碳原子最多有5个
D.充分燃烧等质量的X和甲烷,X消耗氧气多
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的分子式为C4H8O2,有关其同分异构体数目的说法错误的是( )
A.属于酯类的有4种
B.属于羧酸的有2种
C.既含有羟基又含有醛基的有3种
D.存在分子中含有六元环的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示。下列说法中正确的是( )
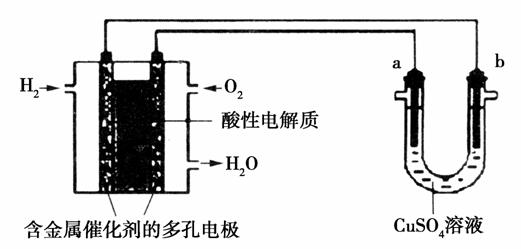
A.燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:2NH3(g)N2(g)+3H2(g) ΔH=+92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质 物质的量/mol | 平衡时反应中的能量变化 | ||
| NH3 | N2 | H2 | ||
| ① | 2 | 0 | 0 | 吸收热量a kJ |
| ② | 0 | 1 | 3 | 放出热量b kJ |
| ③ | 4 | 0 | 0 | 吸收热量c kJ |
下列叙述正确的是( )
A.热量关系:a=b
B.①②③反应的平衡常数:③>①>②
C.达平衡时H2的体积分数:①>③
D.①中的密度不再改变时说明反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
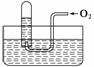 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体是 ( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体是 ( )
A.可能是N2与NO2的混合气体
B.只能是O2与NO2的混合气体
C.可能是NO与NO2的混合气体
D.只能是NO2一种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象不能说明相关结论的是( )
A.将铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性
B.将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低
C.向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl的溶解平衡正向移动
D.向Al(OH)3沉淀中滴加NaOH溶液或盐酸,沉淀均消失,说明Al(OH)3是两性氢氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com