
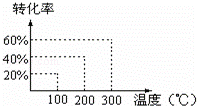
将X和Y以1:2的体积比混合后置于密闭容器中,加压到3×107Pa,发生如下反应:(g)+2Y(g)⇌2Z(g),达到平衡状态时,测得反应物的总物质的量和生成物的总物质的量相等,有关数据如图,则反应对应的温度是( )
|
| A. | 100℃ | B. | 200℃ | C. | 300℃ | D. | 不能确定 |
| 化学平衡的影响因素.. | |
| 专题: | 化学平衡专题. |
| 分析: | 本题目通过求出X或Y的转化率,然后查图象就可以确定其相应温度,令开始加入的X和Y的物质的量分别为1mol、2mol,设达到平衡时,X转化的物质的量为x,根据三段式用x表示出平衡时各组分的物质的量,根据反应物的总物质的量和生成物的总物质的量相等,列方程球x的值,计算x的转化率,结合图象判断. |
| 解答: | 解:令开始加入的X和Y的物质的量分别为1mol、2mol,设达到平衡时,X转化的物质的量为x,则: X(g)+2Y(g)⇌2Z(g) 起始/mol 1 2 0 转化/mol x 2x 2x 平衡/mol 1﹣x 2﹣2x 2x 所以有1﹣x+2﹣2x=2x,解得x=0.6mol. 故X和Y的转化率均为 故选C. |
| 点评: | 本题考查化学平衡的有关计算,难度不大,清楚求出X或Y的转化率,然后查图象就可以确定其相应温度是解题的关键,注意三段式解题法的运用. |


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
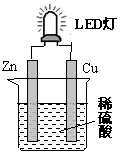
右图是课外活动小组设计的用化学电源使LED灯
发光的装置。下列说法错误的是
A.铜片表面有气泡生成
B.装置中存在“化学能→ 电能→ 光能”的转换
C.如果将硫酸换成柠檬汁,导线中不会有电子流动
D.如果将锌片换成铁片,电路中的电流方向不变
查看答案和解析>>
科目:高中化学 来源: 题型:
锑(Sb)在自然界中一般以硫化物的形式存在,我国锑的蕴藏量占世界第一.从硫化物中提取单质锑一般先在高温下将硫化物转化为氧化物,再用碳还原:关于反应①、②的说法正确的是( )
①2Sb2S3+3O2+6Fe Sb4O6+6FeS,
Sb4O6+6FeS,
②Sb4O6+6C 4Sb+6CO↑.
4Sb+6CO↑.
|
| A. | 反应①、②中的氧化剂分别是Sb2S3、Sb4O6 |
|
| B. | 反应①中每生成3molFeS时,共转移6 mol电子 |
|
| C. | 反应②说明高温下Sb的还原性比C强 |
|
| D. | 每生成4 molSb时,反应①与反应②中还原剂的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机、轮船等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常见非金属单质;常温下C、F、I、E、J和K为气体;E对空气的相对密度为0.586;G为液体.有关物质间的转化关系如下(图中部分反应物或产物已省略):
请填空
(1)B的电子式 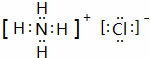 ,B物质的水溶液呈 酸性 ,原因是 NH4++H20⇌NH3.H2O+H+ (用离子方程式表示)
,B物质的水溶液呈 酸性 ,原因是 NH4++H20⇌NH3.H2O+H+ (用离子方程式表示)
(2)反应①的离子反应方程式为 Mg+2NH4+=Mg2++2NH3↑+H2↑
(3)操作a必须在HCl气流中加热得无水物,其原因是 抑制Mg2+的水解 ;操作b为 熔融状态下电解
(4)K+G+F→L写出该反应的化学方程式 4NO2+O2+2H2O=4HNO3 ,
(5)已知C的燃烧热为286KJ/mol,请写出表示1g C在F中完全燃烧生成液体G的热化学反应方程式 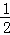 H2(g)+
H2(g)+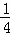 O2(g)=
O2(g)=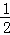 H2O(l)△H=﹣143kJ/mol .
H2O(l)△H=﹣143kJ/mol .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
|
| A. | 铁制品上电镀锌时,理论上电镀液ZnCl2需要不断更换 |
|
| B. | 钢铁设备与外加直流电源的正极相连可以防止钢铁腐蚀 |
|
| C. | 甲烷燃料(KOH)电池的正极反应为:O2+2H2O+4e﹣=4OH﹣ |
|
| D. | 粗铜精炼过程中,电路中每通过2mol电子,阳极就会溶解64g铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在1L恒容密闭容器中充入1mol Z发生反应:2Z(g)═2X(g)+Y(g),反应过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示.下列推断正确的是( )

|
| A. | 升高温度,平衡常数减小 |
|
| B. | Z在a、c两点的反应速率相等 |
|
| C. | b点时,Z的转化率最小 |
|
| D. | 平衡时充入惰性气体时,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
电化学与生产生活密切相关.请运用相关知识回答下列问题:
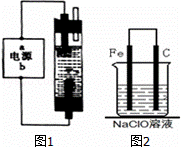
(1)如图1为某同学设计的装置,用石墨作电极电解饱和氯化钠溶液制备家用环保型消毒液(NaClO溶液)发生器.
若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,
则电源的a电极名称为 极(填“正”、“负”、“阴”或“阳”),
装置溶液中反应生成NaClO的离子方程式为: .
(2)该消毒液还具有的化学性质是 (填序号).
A.强氧化性 B.强还原性 C.不稳定性 D.漂白性E.弱酸性
(3)设计方案,对该消毒液对碳钢制品的腐蚀原理实施探究.
①用烧杯取少量样品,将一颗光亮的普通碳钢钉放入烧杯,浸泡一段时间.预期的实验现象是 .
②为了进一步探究铁钉在该漂白剂(NaClO)溶液中的腐蚀原理,现设计了如图2实验装置,请写出碳(C)极上发生的电极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
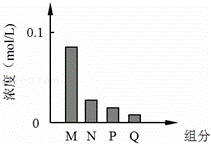
常温下,将10mL 0.2mol/L的一元酸HA与V mL等浓度的NaOH溶液混合.当V=10mL时,所得溶液中部分微粒组成及浓度如图所示.假设溶液体积可以相加,则下列说法正确的是( )
|
| A. | 图中N表示HA,P表示OH﹣,Q表示H+ | B. | 若V=10 mL,则pH=7 |
|
| C. | 若V<10 mL,则溶液显酸性 | D. | 若V=10 mL,则:c(M)+c(P)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能. 已知部分化学键的键能如下:
| 化学键 | N—H | N—N | O==O | N≡N | O—H |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
发射神舟飞船的长征火箭用了肼(N2H4,气态)为燃料,若它在氧气(气态)中燃烧,生成N2(气态)和H2O(液态).1 mol肼完全燃烧时放出的热量为________ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com