
| 点燃 |
| 点燃 |
| A、减少空气进入量,增大天然气进量 |
| B、减少空气进入量,减少天然气进量 |
| C、增大空气进入量,增大天然气进量 |
| D、增大空气进入量,减少天然气进量 |
| 点燃 |
| 点燃 |


科目:高中化学 来源: 题型:
| A、为增强水的导电性,常在水中加入一定量的稀硫酸或氢氧化钠溶液 |
| B、在水电解器中加满水,然后接通直流电源 |
| C、电解水的实验证明水是由氢、氧两种元索组成的 |
| D、与电源正极相连的玻璃管内得到的气体能在空气中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向20mL某物质的量浓度的AlCl3溶液中滴入2mol/L NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
向20mL某物质的量浓度的AlCl3溶液中滴入2mol/L NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1molFe与0.1molCl2充分反应转移电子数为0.2NA |
| B、16g甲基正离子(13CH3+)所含电子数为9NA |
| C、关于反应:C2H2(g)+2.5O2(g)→2CO2(g)+H2O(1)+1300kJ,若CO2中有4NA对共用电子对生成,则放出热量为1300kJ |
| D、0.lmol/LFe2(SO4)3溶液200mL中阴离子和阳离子总数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Na+、CO32-、Cl- |
| B、Ba2+、Na+、Cl-、SO42- |
| C、Ag+、Al3+、NO3-、H+ |
| D、K+、H+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高二上学期期末考试化学试卷(解析版) 题型:填空题
(10分) Ⅰ、在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:

①A中反应的离子方程式为:_______________________________。
②B中Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。
③比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
Ⅱ、如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
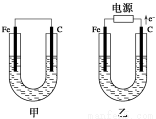
(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的________棒。
②乙池中阳极的电极反应式是___________________。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①甲池中碳棒上电极反应式是_____________________,
②乙池电解一段时间后,测知溶液体积为200ml,PH=13,则阴极生成的气体在标准状况下体积是______L。
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省高二上学期期末考试化学试卷(解析版) 题型:选择题
在铁制品上镀上一层锌层,以下电镀方案中合理的是
A.锌作阳极,铁制品作阴极,溶液中含Fe2+
B.锌作阴极,铁制品作阳极,溶液中含Zn2+
C.锌作阴极,铁制品作阳极,溶液中含Fe3+
D.锌作阳极,铁制品作阴极,溶液中含Zn2+
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(理)试卷(解析版) 题型:填空题
(14分)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层。
(1)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。

该结构中,
①氮镍之间形成的化学键是________;从原子轨道重叠的方式看,碳碳之间的共价键类型是σ键,则碳氮之间的共价键类型是 。
②碳原子的杂化轨道类型有 。
③氧氢两元素之间除共价键外还可能存在_______________;
(2)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= ;CO与N2互为等电子体.CO的总键能大于N2的总键能,但CO比N2容易参加化学反应.根据下表数据,说明CO比N2活泼的原因是 。

(3)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O—C—H键角 (填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com