
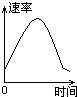
 对可逆反应:A(g)+2B(s)?C(s)+D(g);△H>0(正反应为吸热反应).如图所示为正、逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:①加入A;②加入催化剂;③加压;④升温;⑤减少C,符合图示的条件是( )
对可逆反应:A(g)+2B(s)?C(s)+D(g);△H>0(正反应为吸热反应).如图所示为正、逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:①加入A;②加入催化剂;③加压;④升温;⑤减少C,符合图示的条件是( )| A、②③ | B、①② | C、③④ | D、④⑤ |


科目:高中化学 来源: 题型:
| A、①②④ | B、③④⑤ |
| C、②③④ | D、②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH+H2O?CH3COO-+H3O+ |
| B、CO2+H2O?HCO3-+H+ |
| C、F-+H2O?HF+OH- |
| D、HS-+H2O?S2-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.24mol |
| B、0.21mol |
| C、0.18mol |
| D、0.14mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
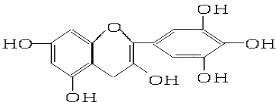 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )| A、①② | B、①④ | C、②④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2NaIO3+5NaHSO3═3NaHSO4+2Na2SO4+I2+H2O.
2NaIO3+5NaHSO3═3NaHSO4+2Na2SO4+I2+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要480mL 0.4mol?L-1的NaCl溶液,有如下操作步骤:
实验室需要480mL 0.4mol?L-1的NaCl溶液,有如下操作步骤:查看答案和解析>>
科目:高中化学 来源: 题型:
A、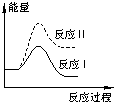 |
B、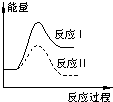 |
C、 |
D、 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com