
 2SO3£¬ÕāŹĒŅ»øö·ÅČȵÄæÉÄę·“Ó¦”£Čē¹ū·“Ó¦ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ£¬“ķĪóµÄŹĒ£Ø £©
2SO3£¬ÕāŹĒŅ»øö·ÅČȵÄæÉÄę·“Ó¦”£Čē¹ū·“Ó¦ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ£¬“ķĪóµÄŹĒ£Ø £©| A£®ŌŚÉĻŹöĢõ¼žĻĀ£¬SO2²»æÉÄÜ100%µŲ×Ŗ»ÆĪŖSO3 |
| B£®“ļµ½Ę½ŗāŹ±£¬µ„Ī»Ź±¼äÉś³É2a mol SO3£¬Ķ¬Ź±Éś³Éa mol O2 |
| C£®ĪŖĮĖĢįøßSO2µÄ×Ŗ»ÆĀŹ£¬Ó¦ŹŹµ±ĢįøßO2µÄÅØ¶Č |
| D£®“ļµ½Ę½ŗāŹ±£¬SO2µÄÅضČÓėSO3µÄÅضČĻąµČ |
 ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
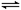 xC(g)£«2D(g)”£2 minÄ©øĆ·“Ó¦“ļµ½Ę½ŗā£¬Éś³É0.8 mol D£¬²¢²āµĆCµÄÅضČĪŖ0.2 mol”¤L£1”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
xC(g)£«2D(g)”£2 minÄ©øĆ·“Ó¦“ļµ½Ę½ŗā£¬Éś³É0.8 mol D£¬²¢²āµĆCµÄÅضČĪŖ0.2 mol”¤L£1”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ| A£®AµÄ×Ŗ»ÆĀŹĪŖ40% |
| B£®2 minÄŚBµÄ·“Ó¦ĖŁĀŹĪŖ0.2 mol”¤(L”¤min)£1 |
| C£®x£½2 |
| D£®Čō»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä£¬Ōņ±ķĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 N2O4£ØĪŽÉ«£©£Ø”÷H<0£©£¬·“Ó¦ÖŠNO2”¢N2O4µÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼£¬°“ĻĀĮŠŅŖĒó×÷“š£ŗ
N2O4£ØĪŽÉ«£©£Ø”÷H<0£©£¬·“Ó¦ÖŠNO2”¢N2O4µÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼£¬°“ĻĀĮŠŅŖĒó×÷“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ļņ0.1 mol/L“×ĖįČÜŅŗÖŠ¼ÓČėÉŁĮæ“×ĖįÄĘČÜŅŗ£¬ČÜŅŗµÄpHŌö“ó |
| B£®Ļņ0.1 mol/L“×ĖįČÜŅŗÖŠ¼ÓČėÉŁĮæNaOHČÜŅŗ£¬ČÜŅŗÖŠc(CH3COO£)¼õÉŁ |
| C£®Ļņ0.1 mol/L“×ĖįČÜŅŗÖŠ²»¶Ļ¼ÓĖ®£¬ČÜŅŗÖŠc(H£«)Ōö“ó |
| D£®Ļņ0.1 mol/L“×ĖįČÜŅŗÖŠµĪČėÉŁĮæÅØŃĪĖį£¬ČÜŅŗµÄµ¼µēŠŌ¼õČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2NH3£¬ĻĀĮŠĖµ·ØÄܱķĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ£Ø £©
2NH3£¬ĻĀĮŠĖµ·ØÄܱķĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ£Ø £©| A£®Éś³É°±µÄĖŁĀŹÓė·Ö½ā°±µÄĖŁĀŹĻąµČ |
| B£®¶ĻæŖŅ»øöN”ŌN£¬Ķ¬Ź±ÓŠĮłøöN-H¼üÉś³É |
| C£®N2”¢H2£¬”¢NH3µÄÅضČĻąµČ |
| D£®»ģŗĻĘųĢå×ÜŃ¹²»ŌŁøıä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®“ņæŖĘūĖ®ĘæŹ±£¬ÓŠ“óĮæĘųÅŻŅē³ö |
B£®¶Ō2HI(g)  H2(g) + I2(g)£¬Ōö“óĘ½ŗāĢåĻµŃ¹ĒææÉŹ¹ŃÕÉ«±äÉī H2(g) + I2(g)£¬Ōö“óĘ½ŗāĢåĻµŃ¹ĒææÉŹ¹ŃÕÉ«±äÉī |
| C£®ŌŚŗĻ³É°±µÄ·“Ó¦ÖŠ£¬ĪŖĢįøßNH3µÄ²śĀŹ£¬²ÉČ”øßŃ¹µÄĢõ¼ž |
D£®äåĖ®ÖŠÓŠBr2 + H2O HBr + HBrO£¬µ±¼ÓČėAgNO3ČÜŅŗŗó£¬ČÜŅŗŃÕÉ«±äĒ³ HBr + HBrO£¬µ±¼ÓČėAgNO3ČÜŅŗŗó£¬ČÜŅŗŃÕÉ«±äĒ³ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 3Z(g)£¬Čō·“Ó¦æŖŹ¼Ź±³äČė2mol XŗĶ2mol Y£¬“ļĘ½ŗāŗóYµÄĢå»ż·ÖŹżĪŖa%”£ĘäĖūĢõ¼ž²»±äŹ±£¬Čō°“ĻĀĮŠĖÄÖÖÅä±Č×÷ĪŖĘšŹ¼ĪļÖŹ£¬Ę½ŗāŗóYµÄĢå»ż·ÖŹż£¾a%µÄŹĒ
3Z(g)£¬Čō·“Ó¦æŖŹ¼Ź±³äČė2mol XŗĶ2mol Y£¬“ļĘ½ŗāŗóYµÄĢå»ż·ÖŹżĪŖa%”£ĘäĖūĢõ¼ž²»±äŹ±£¬Čō°“ĻĀĮŠĖÄÖÖÅä±Č×÷ĪŖĘšŹ¼ĪļÖŹ£¬Ę½ŗāŗóYµÄĢå»ż·ÖŹż£¾a%µÄŹĒ| A£®1molY£¬1molZ | B£®2mol X£¬1molY£¬1molZ | C£®1molYŗĶ3molZ | D£®2molZ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 CO2(g) £«H2(g)£¬“ļµ½Ę½ŗāŹ±²āµĆn(H2)ĪŖ0.5 mol£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
CO2(g) £«H2(g)£¬“ļµ½Ę½ŗāŹ±²āµĆn(H2)ĪŖ0.5 mol£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(””””)| A£®ŌŚøĆĪĀ¶ČĻĀĘ½ŗā³£ŹżK£½1 | B£®Ę½ŗā³£ŹżÓė·“Ó¦ĪĀ¶ČĪŽ¹Ų |
| C£®COµÄ×Ŗ»ÆĀŹĪŖ50% | D£®ĘäĖūĢõ¼ž²»±ä£¬øıäŃ¹ĒæĘ½ŗā²»ŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com