
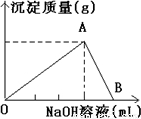
 ,选项中没有图象符合;
,选项中没有图象符合; ,故选b符合;
,故选b符合; ,图象c符合;
,图象c符合;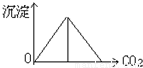 ,图象a符合;
,图象a符合;

科目:高中化学 来源: 题型:

 2NH3的平衡常数K的数值为
2NH3的平衡常数K的数值为查看答案和解析>>
科目:高中化学 来源:09-10学年浠水一中高二下学期期中考试化学卷 题型:选择题
某溶液中发生反应:A=2B+C,A的反应速率v(A)与时间t的图象如图所示。若溶液的体积为2L,且起始时只加入A物质,下列说法错误的是

A.图中阴影部分的面积表示0~2min内A的物质的量浓度的减小值
B.反应开始的前2min,A的平均反应速率小于0.375mol·L-1·min-1
C.至2min时,A的物质的量减小值介于0.5mol至1mol之间
D.至2min时,c(B)介于1mol·L-1 至1.5mol·L-1 之间
查看答案和解析>>
科目:高中化学 来源:2011年山西大学附中高考化学一模试卷(2月份)(解析版) 题型:解答题
 2NH3的平衡常数K的数值为______.保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将______(填“增大”或“减小”或“不变”).保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态______(填“大”或“小”或“不变”).
2NH3的平衡常数K的数值为______.保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将______(填“增大”或“减小”或“不变”).保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态______(填“大”或“小”或“不变”).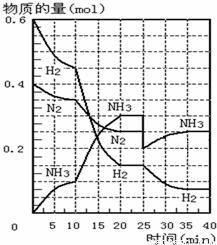
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com