
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)$?_{催化剂}^{500℃、30M}$2NH3(g)?△H=-38.6 kJ•mol-1 | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1 | |
| D. | 2NO2═O2+2NO△H=+116.2 kJ•mol-1 |
分析 A.燃烧热中水为液态;
B.合成氨为可逆反应,热化学方程式中为完全转化时的能量变化;
C.燃烧反应为放热反应,热化学方程式中物质的状态、焓变需标明;
D.未注明物质的状态.
解答 解:A.甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1,故A错误;
B.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,可知1N2和3mol H2置于密闭的容器中充分反应生成NH3(g)放热大于38.6kJ,则热化学方程式为N2(g)+3H2(g)$?_{催化剂}^{500℃、30M}$2NH3(g)△H<-38.6 kJ•mol-1,故B错误;
C.S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1中状态、焓变均合理,故C正确;
D.2NO2═O2+2NO△H=+116.2 kJ•mol-1中未注明物质的状态,故D错误;
故选C.
点评 本题考查热化学方程式,为高频考点,把握燃烧热、热化学方程式的书写为解答的关键,侧重分析与应用能力的考查,注意反应中能量变化与状态、物质的量均有关,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释 | |
| B. | 用铁质自来水管与铜质水龙头连接使用时,连接处的铁水管锈蚀更快 | |
| C. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | |
| D. | 海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:3:1 | B. | 2:2:3 | C. | 1:3:4 | D. | 3:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2CO3溶液显碱性:CO32-+2H2O═H2CO3+2OH- | |
| B. | HS-电离的离子方程式:HS-+H2O═H3O++S2- | |
| C. | 少量氢氧化钙溶液与碳酸氢钠溶液混合,反应的离子方程式:Ca2++2HCO3-+2OH-═CaCO3+2H2O+CO32- | |
| D. | 在0.5 mol•L-1的K2Cr2O7溶液中存在如下平衡:Cr2O72-+H2O═2CrO42-+2H+,其平衡常数的表达式为$\frac{{{c^2}(CrO_4^{2-})•{c^2}({H^+})}}{{c(C{r_2}O_7^{2-})}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A. | 达平衡后升温,反应速率增大,压强减小 | |
| B. | 其他条件不变,增加压强能提高CO的转化率 | |
| C. | 该反应△H>0 | |
| D. | 830℃时,在2 L的密闭容器中加入4 mol CO(g)和4 mol H2O(g),平衡时,CO的转化率是50% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
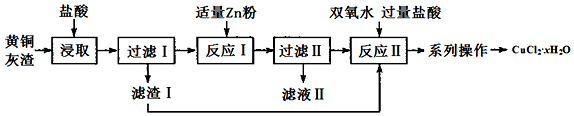
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅是酸性氧化物,不与任何酸反应 | |
| B. | 将氯气通入紫色石蕊试液,先变红,后褪色 | |
| C. | 次氯酸不稳定,见光易分解 | |
| D. | SO2使紫色酸性高锰酸钾溶液褪色,体现了SO2强还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com