
| A����10NA������ת��ʱ���÷�Ӧ����1300kJ������ |
| B����NA��ˮ����������ΪҺ̬ʱ������1300kJ������ |
| C����NA��̼�����õ��Ӷ��γ�ʱ���ų�1300kJ������ |
| D����8NA��̼�����õ��Ӷ��γ�ʱ���ų�1300kJ������ |
 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��C2H4��C2H6 | B��C2H2��C3H8 | C��C2H6��C3H8 | D��C2H6��CH4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���� | B���ڢ� | C���ۢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ===H2O��g�� ��H1��a kJ��
===H2O��g�� ��H1��a kJ��
 ===2H2O��g�� ��H2��b kJ��
===2H2O��g�� ��H2��b kJ��
 ===H2O��l�� ��H3��c kJ��
===H2O��l�� ��H3��c kJ��
 ===2H2O��l�� ��H4��d kJ��
===2H2O��l�� ��H4��d kJ��
| A��a��c ��0 | B��b��d��0 | C��2a��b��0 | D��2c��d��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��2H2O��g������H2��--Q2 kJ��
��2H2O��g������H2��--Q2 kJ��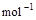 ��
�� ��2H2O��l������H2��--Q3 kJ��
��2H2O��l������H2��--Q3 kJ��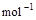 ��
��| A��0.4Q1+0.05Q3 | B��0.4Q1+0.05Q2 | C��0.4Q1+0.1Q3 | D��0.4Q1+0.2Q2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
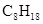 �����飩ȼ�����ɶ�����̼��Һ̬ˮʱ�ų�48.40kJ��������ʾ������Ӧ���Ȼ�ѧ����ʽ��ȷ���ǣ�����
�����飩ȼ�����ɶ�����̼��Һ̬ˮʱ�ų�48.40kJ��������ʾ������Ӧ���Ȼ�ѧ����ʽ��ȷ���ǣ�����A��  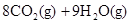 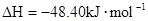 |
B��  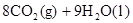 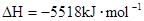 |
C��  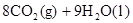 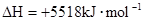 |
D��  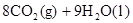 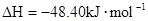 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CH3OH(l)��3/2O2(g)===CO2(g)��2H2O(l)��H����725.8 kJ��mol��1 |
| B��2CH3OH(l)��3O2(g)===2CO2(g)��4H2O(l)��H����1452 kJ��mol��1 |
| C��2CH3OH(l)��3O2(g)===2CO2(g)��4H2O(l)��H����725.8 kJ��mol��1 |
| D��2CH3OH(l)��3O2(g)===2CO2(g)��4H2O(l)��H����1452 kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��a<b | B��a��b |
| C��a>b | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����y kJ��mol��1 |
| B����(10x��y)kJ��mol��1 |
| C����(5x��0��5y)kJ��mol��1 |
| D��(10x��y)kJ��mol��1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com