
如图所示a、b 都是惰性电极,通电—段时间后,a极附近溶液显红色。下列说法中正确的是( )。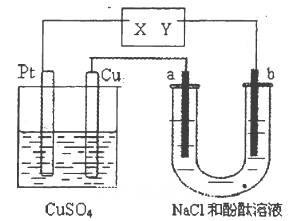
| A.X是正极,Y是负极 | B.X是负极,Y是正极 |
| C.CuSO4溶液的浓度逐渐减小 | D.CuSO4溶液的pH减小 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A.氢氧燃料电池的负极反应式:O2 + 2H2O+ 4e- = 4OH - |
| B.铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S)-2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq) |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- = Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - = Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如图,其中两极区间的隔膜只允许Li+通过。电池充电时的总反应化学方程式为:LiCoO2 = Li1-xCoO2+xLi。关于该电池的推论错误的是
A.放电时,Li+主要从负极区通过隔膜移向正极区
B.放电时,负极反应xLi-xe-= xLi+
C.充电时,有电能转化为化学能
D.充电时,负极(C)上锂元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图为氢氧燃料电池示意图,按此图的提示,下列叙述不正确的是( )。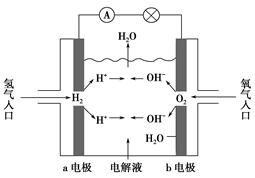
| A.a电极是负极 |
| B.b电极的电极反应为:4OH--4e-=2H2O+O2↑ |
| C.氢氧燃料电池是一种具有应用前景的绿色电源 |
| D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某原电池总反应离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B.正极为C,负极为Fe,电解质溶液为Fe(NO3)3溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
| A.甲醇 | B.天然气 | C.液化石油气 | D.氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某小组为研究电化学原理,设计如图装置。下列叙述正确的是( )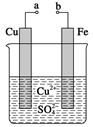
| A.a和b用导线连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为2H++2e-=H2↑ |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
1 L K2SO4和CuSO4的混合溶液中c(S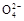 )="2.0" mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
)="2.0" mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
| A.2.0 mol·L-1 | B.1.5 mol·L-1 |
| C.1.0 mol·L-1 | D.0.5 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )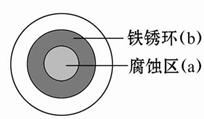
| A.液滴中的Cl-由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com