
【题目】图表示细胞四种有机物的组成。依据生物功能,分析回答下列问题:
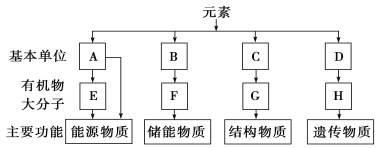
(1)A是指________;E在动物细胞内是指________,在植物细胞内主要是指________。
(2)F是指________;它是由B(脂肪酸和甘油)形成的,除此之外,脂质还包括________ 和________。
(3)C是指________,通式是________;C形成G过程的反应叫________。
(4)D是指________,H是指________。
【答案】葡萄糖糖原淀粉脂肪固醇磷脂氨基酸![]() 脱水缩合脱氧核苷酸DNA
脱水缩合脱氧核苷酸DNA
【解析】
本题以“细胞四种有机物的组成和功能关系图”为载体,考查学生对细胞内的有机大分子的化学组成、功能的掌握情况。
(1) 糖类是主要的能源物质,据此分析图示可知:A是指葡萄糖,E是多糖,动物细胞中的多糖是糖原,在植物细胞中主要是指淀粉。
(2) 脂肪是细胞内良好的储能物质,因此储能物质F是脂肪;脂质除了脂肪外,还包括固醇和磷脂。
(3) 许多蛋白质是组成细胞和生物体结构的重要物质,据此可判断结构物质G是蛋白质,其基本组成单位C是氨基酸,氨基酸结构通式见答案。氨基酸形成蛋白质的反应叫脱水缩合。
(4) 在细胞中,遗传物质H为DNA,其基本组成单位D是脱氧核苷酸。


科目:高中化学 来源: 题型:
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)![]() (绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在。Cr(OH)3为难溶于水的灰蓝色固体。回答下列问题:
(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在。Cr(OH)3为难溶于水的灰蓝色固体。回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是________________________;
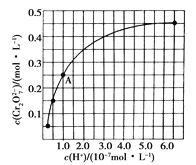
(2)CrO42-和Cr2O72-在溶液中可相互转化。室温下初始浓度为1.0 mol·L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如上图所示。
①用离子方程式表示Na2CrO4溶液中的转化反应_____________________;
②由图可知,溶液酸性增大,CrO42-的平衡转化率________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为___________;
③升高温度,溶液中CrO42-的平衡转化率减小,则该反应的ΔH________0(填“大于”“小于”或“等于”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO42-生成砖红色沉淀,指示滴定终点的到达。当溶液中Cl-恰好沉淀完全(Cl-浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为________mol·L-1,此时溶液中c(CrO![]() )等于________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
)等于________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准浓度的NaOH溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定浓度比实际浓度偏高的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗,②锥形瓶中有少量蒸馏水,实验时没有烘干处理,③取未知浓度盐酸的酸式滴定管用蒸馏水洗净后,未用待测盐酸润洗,④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失,⑤滴定后读数时,俯视读数.
A. ①④ B. ②③ C. ①③ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是 ( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是 ( )
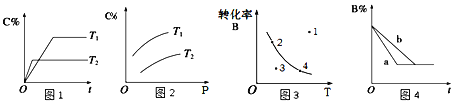
A. 由图1可知,T1<T2,该反应正反应为吸热反应
B. 由图2可知,该反应m+n﹤p
C. 图3中,表示反应速率v正>v逆的是点3
D. 图4中,若m+n=p,则a曲线一定使用了催化剂
【答案】C
【解析】A. 由图1可知,T2时达到平衡所需时间短,所以T1<T2,升温平衡左移,该反应正反应为放热反应,故A错误;B. 由图2可知,加压平衡右移,说明该反应m+n>p,故B错误;C. 图3中,温度一定,点3达到平衡的过程中B减少,V正>V逆,故C正确;D. 图4中,若m+n=p,加压平衡不移动,则a曲线可能为加压,故D错误。故选C。
点睛:在分析本题图1和图4一类涉及影响反应速率条件的图像时,注意把握图像的关键内容—斜线的斜率,斜率越大,反应速率越大,对应的是有利于增大反应速率的条件。
【题型】单选题
【结束】
11
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行反应:X(g)+2Y(g)![]() 3Z(g)+Q(s) △H >0,下列叙述正确的是
3Z(g)+Q(s) △H >0,下列叙述正确的是
A. 当容器中X与Y的物质的量的比满足1:2时反应达到平衡
B. 达到平衡时X的转化率为25%,则平衡常数K值为9/4
C. 达到平衡后,反应速率2V正(Y)="3" V逆(Z)
D. 达到平衡后,加入Q,平衡逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同物质的量的SO2和SO3 , 下列说法中正确的是( )
A.硫元素的质量比为5:4
B.任何情况下体积比均为1:1
C.含有的O2、O3两分子数之比为1:1
D.SO2、SO3两分子数之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如下装置制取氮气,并用氮气制备Ca3N2,Ca3N2遇水发生水解反应。下列说法错误的是
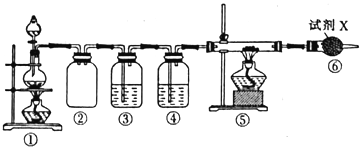
A. ①中发生的化学反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B. ④、⑥中依次盛装的试剂可以是浓H2SO4、碱石灰
C. ③中盛放的试剂是NaOH 溶液
D. 实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子, X、Y、Z、P分别为构成生物大分子的基本单位,请回答下列问题:
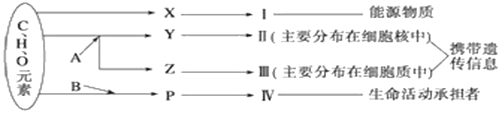
(1)Ⅰ在小麦种子中主要是指______,其基本单位X是______。
(2)A代表的元素是____,Ⅱ是____,Ⅲ是RNA,Z是_____。
(3)Ⅳ一定含有的元素有______。P的结构通式是______,图中由P形成Ⅳ的反应方式称为____,Ⅳ的特定功能的发挥与其_____结构有关。若P的平均相对分子质量r,由多个P形成m条肽链,经盘曲折叠形成了相对分子质量为e的Ⅳ,则Ⅳ分子中肽键的数目是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4)。25℃时,草酸的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;碳酸(H2CO3)的电离平衡常数为K1=4.5×10-7,K2=4.7×10-11。草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:
(1)写出水溶液中草酸的电离方程式_____________________________________ 。
(2)相同条件下物质的量浓度都为0.1mol/L的Na2C2O4溶液的pH比Na2CO3溶液的pH______________ (填“大”、“小”或“相等”) 。
(3)常温下将0.4mol/L的KOH溶液20mL与0.2mol/L的草酸溶液20mL混合,则混合后溶液中阴离子浓度的大小顺序为_____________________________________ 。
(4)往Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为________________。
(5)25℃时,向20mL碳酸钙的饱和溶液中逐滴加入c mol/L的草酸钾溶液20mL后,有草酸钙沉淀生成,则c的最小值为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com