
【题目】配制0.1molL﹣1NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是( )
A.称量时,左盘低,右盘高
B.定容时俯视读取刻度
C.原容量瓶洗净后未干燥
D.定容时液面超过了刻度线
科目:高中化学 来源: 题型:
【题目】丁二酮肟 ![]() 是检验Ni2+的灵敏试剂.
是检验Ni2+的灵敏试剂.
(1)Ni2+基态核外电子排布式为 . 丁二酮肟分子中C原子轨道杂类型为 , 1mol丁二酮肟分子所含σ键的数目为 .
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点﹣19.3℃,沸点42.1℃,易溶于有机溶剂.
①Ni(CO)4固态时属于晶体(填晶体类型).
②与CO互为等电子体的阴离子为(填化学式).
(3)Ni2+与Mg2+、O2﹣形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.在20℃,1.01×105Pa时,22.4L甲烷(CH4)所含的原子数为5NA
B.常温常压下,28g氮气所含的原子数为2NA
C.标准状况下,22.4L水所含有的分子数目为NA
D.0.5mol H2O所含的电子数目为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,在日常生活中有着广泛的应用.工业上用CO生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g),图1表示反应中能量的变化;图二表示一定温度下反应过程: 
根据题意完成下列各题:
(1)图一表示使用和未使用催化剂时反应过程和能量的对应关系.下列有关催化剂的说法不正确是
A.降低分子的能量
B.增加了活化分子数
C.提高了活化分子百分数
D.增加了单位体积内的活化分子数
(2)反应达到平衡时,平衡常数表达式K= , 升高温度,K值(填“增大”、“减小”或“不变”).
(3)在500℃,从反应开始到平衡,氢气的平均反应速率v (H2)=[用n(B)、t(B) 表示].
(4)在其他条件不变的情况下,对处于E点的体系将体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时 ![]() 增大
增大
(5)在T2℃下,将2molCO和6molH2充入2L的密闭容器中,达到平衡状态时,测得c(CO)=0.2molL﹣1 , 则CO的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)某温度下,纯水中的c(H+)=2.0×10﹣7mol/L,此时溶液的c(OH﹣)=mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10﹣4mol/L,则溶液中,由水电离产生的c(H+)=mol/L,此时温度25℃(填“高于”、“低于”或“等于”).
(2)某温度下的水溶液中,C (H+)=10x mol/L,C (OH﹣)=10y mol/L,x和y的关系如图所示.计算:该温度下水的离子积为 . 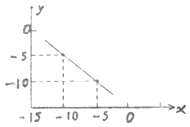
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验. 
图一可通过观察①定性比较得出结论.有同学提出将CuSO4改为CuCl2更为合理,其理由是② , 你认为还可以作何改进?③
(2)图二为在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线,请回答:
(i)“O”点导电能力为O的理由是;
(ii)a、b、c三点的c(H+)由小到大的顺序为;
(iii)a、b、c三点处,电离程度最大的是;
(iv)若使c点溶液中c(CH3COO﹣)增大,c(H+)减小,则可采取的措施是:①;② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知异丙苯的结构简式如图,下列说法错误的是( ) ![]()
A.异丙苯的分子式为C9H12
B.异丙苯的沸点比苯高
C.异丙苯中碳原子可能都处于同一平面
D.异丙苯和苯为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知异丙苯的结构简式如图,下列说法错误的是( ) ![]()
A.异丙苯的分子式为C9H12
B.异丙苯的沸点比苯高
C.异丙苯中碳原子可能都处于同一平面
D.异丙苯和苯为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com