
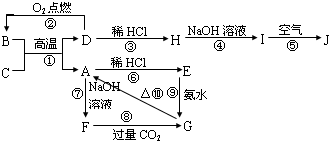
 A~J分别表示中学化学中常见的一种物质,其中A为难熔的主族元素的氧化物,B为黑色晶体.它们之间的相互关系如右图所示:
A~J分别表示中学化学中常见的一种物质,其中A为难熔的主族元素的氧化物,B为黑色晶体.它们之间的相互关系如右图所示:
| ||
| ||
| 2 |
| 3 |
| 2 |
| 3 |
| 8 |
| 3 |
| 8 |
| 3 |


科目:高中化学 来源: 题型:
| A、无论该溶液呈酸性还是碱性,都有c(Na+)+c(H+)=c(A-)+c(OH-) |
| B、无论该溶液呈酸性还是碱性,都有c(Na+)=c(A-)+c(HA) |
| C、若该溶液中HA电离能力大于A-水解能力,则有c(A'>c(Na+)>c(HA)>c(H,>c(OH- |
| D、若该溶液中A-水解能力大于HA电离能力,则有c(A-)>c(Na+)>c(HA)>c(OH-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,36g C5H10分子中一定含有7NA个共用电子对 |
| B、6g尿素与葡萄糖的混合物在足量氧气中完全燃烧生成0.2NA个水分子 |
| C、10mL5mol/L (NH4)2SO4溶液中含有NH4+数目为0.1NA个 |
| D、1mol FeCl3充分转化为Fe(OH)3胶体后形成NA个胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaNO2是还原剂 |
| B、维生素C是还原剂 |
| C、维生素C能将 NaNO2还原 |
| D、NaNO2被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、仅①② | B、仅④⑤ |
| C、仅①③ | D、仅③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com