
| A.金属晶体 | B.原子晶体 | C.离子晶体 | D.分子晶体 |
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.溴、碘是单质,四氯化碳是化合物? |
| B.Cl2、Br2、I2是非极性分子,CCl4也是非极性分子,而水是极性分子? |
| C.溴、碘单质和四氯化碳中都含有卤素? |
| D.Br2、I2常温下都不是气态,CCl4也不是气态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
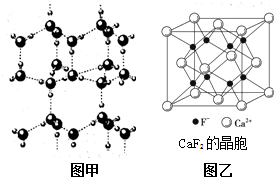
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
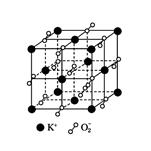
| A.晶体中,0价氧与-2价氧的数目比为2:1 |
| B.晶体中每个K+周围有8个O2-,每个O2-周围有8个K+ |
| C.晶体中与每个K+距离最近的K+有8个 |
| D.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
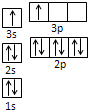
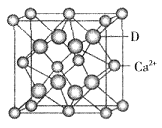
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.非晶体是不稳定的,处于晶体时能量小 |
| B.晶体是稳定的,处于晶体时能量大 |
| C.非晶体是不稳定的,处于晶体时能量小 |
| D.晶体是不稳定的,处于晶体时能量小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com