
【题目】锌是人体必需的微量元素,明朝《天工开物》中有世界上最早的关于炼锌技术的记载。回答下列问题:
(1)基态Zn原子的价电子排布式为____________,在周期表中位置为________________。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除H外其余元素的第一电离能由大到小排序为________________________。
②在[Zn(NH3)4]SO4溶液中滴加NaOH溶液,未出现浑浊,其原因是___________________________。
③已知[Zn(NH3)4]2+的空间构型与SO42-相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为________。
④以下作用力在[Zn(NH3)4]SO4晶体中存在的有________。
A.离子键 B.极性共价键 C.非极性共价键
D.配位键 E.范德华力 F.金属键
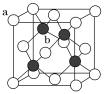
(3)ZnS晶胞结构如图(已知a为硫离子,b为锌离子)所示,ZnS晶体的熔点约为1 700 ℃。
①已知晶体密度为ρ g·cm-3,NA为阿伏加德罗常数的值。则1个ZnS晶胞的体积为________cm3。
②ZnO与ZnS结构相似,熔点为1 975 ℃,其熔点较高的原因是_____________________________。
【答案】3d104s2 第四周期ⅡB族 N>O>S>Zn [Zn(NH3)4]2+难电离,溶液中Zn2+浓度很小,无法产生沉淀 sp3 ABD ![]() O2-的半径比S2-的小,ZnO晶体的晶格能较大
O2-的半径比S2-的小,ZnO晶体的晶格能较大
【解析】
(1)基态Zn原子的电子排布式为1s22s22p63s23p63d104s2,由此可确定基态Zn原子的价电子排布式和其在周期表中位置。
(2)①一般情况下,元素的非金属性越强,第一电离能越大,但N的2p轨道半充满,处于较稳定状态,所以第一电离能出现反常,其第一电离能比O大;Zn为金属,其第一电离能比非金属小。②[Zn(NH3)4]2+中,Zn2+与NH3结合力强,难以发生电离,所以溶液中Zn2+浓度很小,无法产生沉淀。③[Zn(NH3)4]2+的空间构型为正四面体,由此可确定Zn2+的杂化类型。④[Zn(NH3)4]SO4中含有离子键、极性共价键、配位键。(3) 由题图知,一个ZnS晶胞中含有4个Zn2+,含S2-的个数为8×![]() +6×
+6×![]() =4,1个ZnS晶胞的质量为
=4,1个ZnS晶胞的质量为![]() g,由此可求出1个ZnS晶胞的体积。②O2-的半径比S2-的小,故ZnO晶体的晶格能较大。
g,由此可求出1个ZnS晶胞的体积。②O2-的半径比S2-的小,故ZnO晶体的晶格能较大。
(1)基态Zn原子的价电子排布式为3d104s2,在周期表中位置为第四周期ⅡB族。答案为:3d104s2;第四周期ⅡB族;
(2)①一般情况下,元素的非金属性越强,第一电离能越大,但N的2p轨道半充满,处于较稳定状态,所以第一电离能出现反常,其第一电离能比O大;Zn为金属,其第一电离能比非金属小,故N、O、S、Zn的第一电离能由大到小的顺序为N>O>S>Zn。答案为:N>O>S>Zn;
②[Zn(NH3)4]2+中,Zn2+与NH3结合力强,难以发生电离,所以溶液中Zn2+浓度很小,无法产生沉淀。答案为:[Zn(NH3)4]2+难电离,溶液中Zn2+浓度很小,无法产生沉淀;
③[Zn(NH3)4]2+的空间构型为正四面体,Zn2+的杂化类型为sp3杂化。答案为:sp3;
④[Zn(NH3)4]SO4中含有离子键、极性共价键、配位键。答案为:ABD;
(3)①由题图知,一个ZnS晶胞中含有4个Zn2+,含S2-的个数为8×![]() +6×
+6×![]() =4,1个ZnS晶胞的质量为
=4,1个ZnS晶胞的质量为![]() g,故1个ZnS晶胞的体积为
g,故1个ZnS晶胞的体积为![]() cm3。答案为:
cm3。答案为:![]() ;
;
②O2-的半径比S2-的小,故ZnO晶体的晶格能较大,熔点较高。答案为:O2-的半径比S2-的小,ZnO晶体的晶格能较大。


科目:高中化学 来源: 题型:
【题目】H2是一种重要的清洁能源。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2=-49.0kJ/mol,
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.1kJ/mol,H2还原CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) ΔH1,则ΔH1=___kJ/mol,该反应自发进行的条件为_____。
CH3OH(g) ΔH1,则ΔH1=___kJ/mol,该反应自发进行的条件为_____。
A.高温 B.低温 C.任何温度条件下
(2)恒温恒压下,在容积可变的密闭容器中加入1molCO和2.2molH2,发生反应CO(g)+2H2(g)![]() CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。
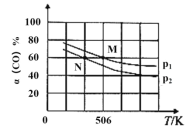
①压强:p1____p2。(填“>”<”或“=”)
②M点时,H2的转化率为_____(计算结果精确到0.1%), 该反应的平衡常数Kp=____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③下列各项能作为判断该反应达到平衡标志的是______(填字母);
A.容器内压强保持不变 B.2v正(H2)=v逆(CH3OH)
C.混合气体的相对分子质量保持不变 D.混合气体的密度保持不变
(3)H2还原NO的反应为2NO(g)+2H2(g)![]() N2(g)+2H2O(1),实验测得反应速率的表达式为v=kcm(NO)·cn(H2)(k是速率常数,只与温度有关)
N2(g)+2H2O(1),实验测得反应速率的表达式为v=kcm(NO)·cn(H2)(k是速率常数,只与温度有关)
①某温度下,反应速率与反应物浓度的变化关系如下表所示。
编号 | c(NO)/(mol/L) | c(H2)/(mol/L) | v/(mol·L-1·min-1) |
1 | 0.10 | 0.10 | 0.414 |
2 | 0.10 | 0.20 | 1.656 |
3 | 0.50 | 0.10 | 2.070 |
由表中数据可知,m=_____,n=_____。
②上述反应分两步进行:i.2NO(g)+H2(g)=N2(g)+H2O2(1)(慢反应);ii
A.H2O2是该反应的催化剂 B.反应i的活化能较高
C.总反应速率由反应ii的速率决定 D.反应i中NO和H2的碰撞仅部分有效
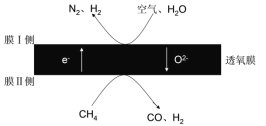
(4)2018年我国某科研团队利用透氧膜,一步即获得合成氨原料和合成液态燃料的原料。其工作原理如图所示(空气中N2与O2的物质的量之比按4:1计)。工作过程中,膜I侧所得![]() =3,则膜I侧的电极方程式为________。
=3,则膜I侧的电极方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌的家用消毒剂其有效成分为对氯间二甲苯酚(结构简式如下图所示),可以杀灭常见的病毒与细菌。下面有关该物质的说法正确的是

A. 该物质的分子式是C8H10ClO
B. 1mol该物质最多可以与2mol NaOH反应
C. 1mol该物质可以与2mol液溴发生取代反应
D. 该物质可以发生加成、取代、消去、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]是透明、浅蓝绿色晶体,易溶于水而不溶于酒精等有机溶剂,在空气中一般比较稳定,不易被氧化。制备步骤如下:
步骤1.称取还原铁粉0.4g,炭粉0.3g,放入50mL 锥形瓶中,加入3.5 mL2mol·L-1硫酸置于60℃ 热水浴中加热(如下左图),待反应完全,取出冷却,再加入6 mol·L-1的硫酸2 mL。

步骤2.在上述反应液中加入浓氨水0.8 mL,振荡混匀,抽滤(如上右图)。向滤液中加入10mL无水乙醇,静置,大量晶体析出,倾析,再次抽滤。
步骤3.取出晶体,用干净的滤纸吸干,称量并分析样品。
请回答下列问题:
(1)步骤1中炭粉的作用是_______,加人6 mol·L-1硫酸的作用是____________。
(2)向滤液中加人无水乙醇目的是_________________。
(3)产品中金属阳离子的检验方法及现象________________。
(4)称取获得的硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](摩尔质量为392g·mol-1)1.9600 g 配成100mL溶液,取出20.00mL滴加稀H2SO4酸化后用0 . 0100 mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液为18.00mL 。
下列有关滴定的操作正确的是_(填字母编号)。
a.滴定过程中眼睛注视滴定管中液面变化
b.滴定完成后取下滴定管握住中部防止掉落
c.读数过程中保持滴定管自然悬垂
d.读数时视线与刻度线、凹液面最低处切线相平齐
滴定过程中反应离子方程式为____________,制得硫酸亚铁钱样品的纯度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
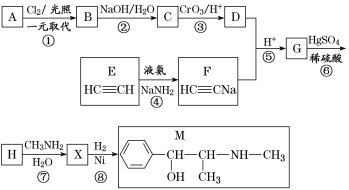
已知:Ⅰ.芳香烃A的相对分子质量为92
Ⅱ.R—CH2OH![]() RCHO
RCHO
III、R1-CHO+
IV、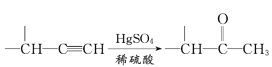
V、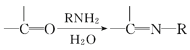
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题(Cl2易溶于CCl4)。
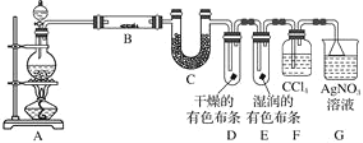
(1)若用含有7.3 g HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2质量总是小于3.55 g的原因是________________________________。
(2)①装置B中盛放的试剂名称为________________,作用是________________________________,现象是_____________________________。
②装置D和E中出现的不同现象说明的问题是___________________。
③装置F的作用是__________________________________________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应放入________(填写试剂或用品名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)已知X、Y、Z、M、G、Q是六种短周期元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)Y、Z、M、G四种元素原子半径由大到小的顺序是(写元素符号) 。
(2)Z在元素周期表中的位置为 。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式) 。
(4)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式) ,在实验室中,制取该物质的反应原理是(写化学方程式) 。
(5)M2Z的电子式为 。MX与水反应可放出气体,该反应的化学方程式为 。
(6)常温下,不能与G的单质发生反应的是(填序号) 。
a.CuSO4溶液 b.Fe2O3c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
工业上用电解法制G的单质的化学方程式是 ,若以石墨为电极,阳极产生的混合气体的成分是(写化学式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题:Ⅰ.下列实验设计或操作合理的是____________。
A.在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
B.只用水就能鉴别苯、硝基苯、乙醇
C.实验室制取乙烯时温度计的水银球在反应液上方
D.将10滴溴乙烷加入1 mL10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子
E.工业酒精制取无水酒精时先加生石灰然后蒸馏,蒸馏必须将温度计的水银球插入反应液中,测定反应液的温度
F.苯酚中滴加少量的稀溴水,可用来定量检验苯酚
G.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验
Ⅱ.学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究。
(1)张老师用如图所示装置进行实验:该实验的目的是__________;课上你所观察到的现象是_____;盛水试管(装置)的作用是________。
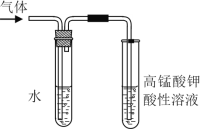
(2)若你用另一实验来达到张老师演示实验的目的,你设计的实验方案依据的反应原理是________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.FeCl3溶液与Cu的反应:Fe3++Cu=Fe2++Cu2+
B.AgNO3溶液与NaCl溶液的反应:Ag++Cl-=AgCl↓
C.Cu(OH)2与CH3COOH溶液的反应:OH-+H+=H2O
D.CaCO3与HNO3溶液的反应:![]() +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com