
 Ⅰ.写出下列化学方程式:
Ⅰ.写出下列化学方程式:分析 Ⅰ.(1)Al和KOH溶液反应的化学方程式为:2Al+2H2O+2KOH═2KAlO2+3H2↑;
(2)Fe和水蒸汽反应的化学方程式为:3Fe+4H2O(g)═Fe3O4+4H2;
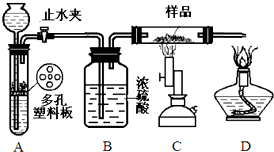
Ⅱ.(1)依据装置分析判断是加热碳酸氢钠固体的反应;
(2)B中盛的是浓硫酸起到吸收水蒸气干燥二氧化碳气体;
(3)过氧化钠和二氧化碳反应生成碳酸钠和氧气;
(4)过氧化钠是淡黄色固体,随反应进行变为白色固体反应生成氧气,蚊香燃烧更剧烈;
(5)氧化钠和二氧化碳反应生成碳酸钠,无氧气生成,蚊香逐渐熄灭.
解答 解:Ⅰ.(1)Al和KOH溶液反应的化学方程式为:2Al+2H2O+2KOH═2KAlO2+3H2↑,故答案为:2Al+2H2O+2KOH═2KAlO2+3H2↑;
(2)Fe和水蒸汽反应的化学方程式为:3Fe+4H2O(g)═Fe3O4+4H2,故答案为:3Fe+4H2O(g)═Fe3O4+4H2;
Ⅱ.(1)依据装置分析判断是加热碳酸氢钠固体的反应生成碳酸钠和二氧化碳水;
反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(2)B中盛的是浓硫酸起到吸收水蒸气干燥二氧化碳气体;故答案为:吸收气体中的水蒸气(干燥CO2);
(3)过氧化钠和二氧化碳反应生成碳酸钠和氧气;反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(4)过氧化钠是淡黄色固体,随反应进行变为白色固体碳酸钠,反应生成氧气具有助燃性,蚊香燃烧更剧烈;上述实验现象说明:Na2O2能与CO2反应,生成白色粉末状物质和O2,故答案为:淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈;Na2O2能与CO2反应,生成白色粉末状物质和O2;
(5)氧化钠和二氧化碳反应生成碳酸钠,无氧气生成,在二氧化碳环境,蚊香逐渐熄灭;
故答案为:点燃的蚊香逐渐熄灭.
点评 本题考查了实验装置的性质分析判断,装置的作用分析,反应产物的判断,物质性质和反应现象判断是解题关键.题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17 g H2O2中含有9NA个质子 | |
| B. | 1 L 0.1 mol•L-1CuSO4溶液中含0.1NA个Cu2+ | |
| C. | 1 mol Fe 与过量的稀HNO3反应,转移2 NA个电子 | |
| D. | 标准状况下,22.4 L SO3含有3NA氯原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
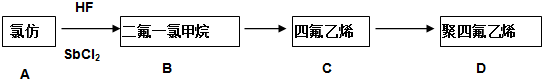
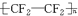 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl- | |
| B. | $\frac{{k}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂 | |
| B. | 在任何条件下都不能发生Cu+H2SO4═CuSO4+H2↑反应 | |
| C. | 浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 | |
| D. | 二氧化氮与水反应的离子方程式是3NO2+H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N和P同一主族,其简单氢化物的沸点NH3>PH3 | |
| B. | 0.5摩尔氧化钠和过氧化钠的混合物中阴阳离子的总数为1.5NA | |
| C. | 在标准状况下22.4L SO3的物质的量约为1摩尔 | |
| D. | 已知P4分子是正四面体结构,31g白磷中含有1.5NA个P-P非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示.
中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com