
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓海轮腐蚀 | |
| B. | 钢铁在潮湿空气中生锈,主要发生的是吸氧腐蚀,铁锈的成分是Fe2O3•XH2O | |
| C. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| D. | 吸热反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)在一定条件下可自发进行,则该反应的△S<0 |
分析 A、Cu与Fe形成原电池时,铜的金属活泼性比铁的弱,铁作负极,被腐蚀;
B、钢铁在潮湿的空气中,由于铁比碳活泼,水膜显中性,则发生吸氧腐蚀;
C、硝酸和锌反应生成氮氧化物;
D、根据△G=△H-T•△S<0自发判断.
解答 解:A、Cu与Fe形成原电池时,铜的金属活泼性比铁的弱,铁作负极,被腐蚀,所以不能在海轮外壳上镶入若干铜块以减缓其腐蚀,故A错误;
B、钢铁在潮湿的空气中,由于水膜为中性或弱酸性,故发生吸氧腐蚀,由于铁比碳活泼,故铁做负极,负极反应为Fe-2e-=Fe2+,碳做正极,发生反应为:O2+4e-+2H2O=4OH-,所以首先形成氢氧化亚铁沉淀,后继续被氧化生成氢氧化铁沉淀,再分解生成铁锈,则铁锈的成分是Fe2O3•XH2O,故B正确;
C、加入硝酸铜时,酸性条件下,硝酸根离子具有强氧化性,能和锌发生氧化还原反应生成氮氧化物,应该加入少量硫酸铜,故C错误.
D、TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)在一定条件下可自发进行,则△G=△H-T•△S<0,又该反应是一个吸热反应,所以△S>0,故D错误.
故选B.
点评 本题考查了一些化学知识在生活中的应用,要根据相关知识点细心分析,注意根据△G=△H-T•△S<0判断反应自发性.


科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2难溶于水,属于非电解质 | |
| B. | SO2能与碱反应生成盐和水,属于酸性氧化物 | |
| C. | NH4Cl组成中不含金属离子,不属于盐 | |
| D. | HCl气体溶于水电离成H+和Cl-,属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含碳元素的化合物都是有机物 | |
| B. | 完全燃烧只生成 CO2和 H2O 的化合物都是烃 | |
| C. | 有机物完全燃烧只可能生成 CO2 和 H2O | |
| D. | 点燃混有空气的甲烷不一定会爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
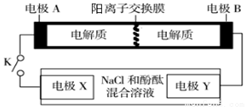 某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )| A. | 放电时,电极A发生还原反应 | |
| B. | A的电极反应式为:3I--2e-=I3- | |
| C. | 当有0.1 mol K+通过离子交换膜,X电极上产生气体1.12 L(标准状况下 | |
| D. | 电池充电时,B电极要与外电源的正极相连,电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
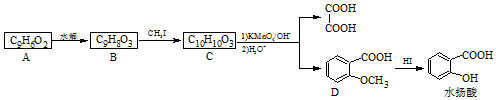

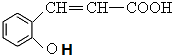 +CH3I→
+CH3I→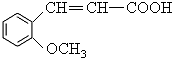 +HI,该反应类型为取代反应,该反应步骤的目的是保护酚羟基,使之不被氧化.
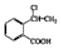
+HI,该反应类型为取代反应,该反应步骤的目的是保护酚羟基,使之不被氧化.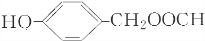 或
或 .
. 合成
合成 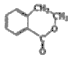 (用反应流程图表示,并注明反应条件).
(用反应流程图表示,并注明反应条件).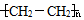
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO4>HClO | B. | 金属性:Na>Mg | ||
| C. | 碱性:KOH>NaOH | D. | 热稳定性:HC1>HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B>A>C | B. | A>B=C | C. | B>A=C | D. | B>C>A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com