
| A. | 由分子组成的物质中不一定存在共价键 | |
| B. | 金刚石、石墨、足球烯均是碳元素的同素异形体,性质都相似 | |
| C. | 由非金属元素组成的晶体一定是分子晶体 | |
| D. | 仅由非金属元素组成的物质不可能含有离子键 |
分析 A.单原子分子中不含共价键;
B.同素异形体是同种元素形成的不同单质,同素异形体物理性质不同,化学性质相似;
C.由非金属元素组成的晶体可能是离子晶体,也可能是分子晶体或原子晶体;
D.仅由非金属元素组成的化合物中可能含有离子键.
解答 解:A.单原子分子中不含共价键,如稀有气体,故A正确;
B.金刚石、石墨、足球烯均是碳元素形成的不同单质,属于同素异形体,物理性质不同,化学性质相似,故B错误;
C.由非金属元素组成的晶体可能是离子晶体,如铵盐,可能是原子晶体,如二氧化硅,故C错误;
D.仅由非金属元素组成的化合物中可能含有离子键,如铵盐,故D错误;
故选A.
点评 本题考查了物质和化学键的关系,不能根据是否含有金属元素判断离子键,稀有气体分子是单原子分子,不存在化学键,为易错点.


科目:高中化学 来源: 题型:解答题
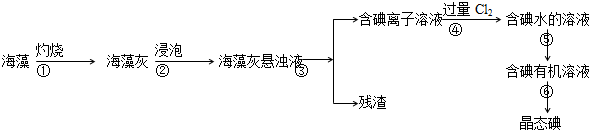
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
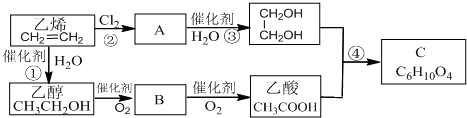
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
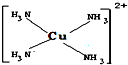 请回答下列问题:
请回答下列问题: (4)请写出HClO的电子式:
(4)请写出HClO的电子式: .
.| 电离能/KJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
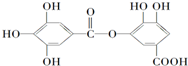
| A. | 在一定条件下,1 mol该物质最多能与6 mol NaOH完全反应 | |
| B. | 有弱酸性,1 mol该有机物与溴水反应,最多能消耗4 mol Br2 | |
| C. | 在Ni催化下,1 mol该物质可以和7 mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量金属钠保存在煤油中 | |
| B. | 少量NaOH保存在带有玻璃塞的试剂瓶中 | |
| C. | 少量白磷保存在冷水中 | |
| D. | 少量浓硝酸保存在棕色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 可制得14.2g氯气 | B. | 被氧化的HCl的质量为14.6g | ||
| C. | 被氧化的HCl的质量为7.3g | D. | 转移的电子的物质的量为0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
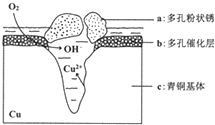 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com