考点:物质的量的相关计算
专题:计算题
分析:(1)钡离子物质的量等于氢氧化钡的物质的量,而氢氧根物质的量等于氢氧化钡的2倍,根据N=nN
A计算Ba
2+、OH
-离子数目;根据m=nM计算25mol Ba(OH)
2的质量;
(2)计算氨气含有原子物质的量,进而计算水的物质的量,再根据N=nN
A计算水分子数目;
(3)n(SO
42-)=
n(Al
3+),根据m=nM计算SO
42-的质量;
(4)存在平衡2NO
2?N
2O
4,只有NO
2时含有分子数目最多,只有N
2O
4时含有分子数目最少,NO
2和N
2O
4混合气体中O元素质量分数为
,据此计算氧原子质量,再根据n=
计算O原子物质的量,再根据N=nN
A计算O原子数目.
解答:
解:(1)n(Ba
2+)=n[Ba(OH)
2]=2.5mol,故含有Ba
2+离子数目=2.5mol×6.02×10
23mol
-1=1.505×10
24,n(OH
-)=2n[Ba(OH)
2]=2×2.5mol=5mol,故含有OH
-离子数目=5mol×6.02×10
23mol
-1=3.01×10
24,
25mol Ba(OH)
2的质量=25mol×171g/mol=4275g;
故答案为:1.505×10
24;3.01×10
24;4275;
(2)0.3mol氨气含有原子物质的量=0.3mol×4=1.2mol,与0.3mol氨气含原子数相等的H
2O的物质的量=
=0.4mol,故水分子数目=0.4mol×6.02×10
23mol
-1=2.408×10
23,
故答案为:2.408×10
23;
(3)n(SO
42-)=
n(Al
3+)=
×0.4mol=0.6mol,SO
42-的质量=0.6mol×96g/mol=57.6g,
故答案为:57.6;
(4)存在平衡2NO
2?N
2O
4,只有NO
2时含有分子数目最多,分子数最多接近为
×6.02×10
23mol
-1=6.02×10
23,只有N
2O
4时含有分子数目最少,分子数最少接近为
×6.02×10
23mol
-1=3.01×10
23,
NO
2和N
2O
4混合气体中O元素质量分数为
,氧原子质量=46g×
=32g,O原子物质的量=
=2mol,故含有O原子数目=2mol×6.02×10
23mol
-1=1.204×10
24,
故答案为:6.02×10
23;3.01×10
23;1.204×10
24.
点评:本题考查物质的量有关计算,比较基础,(4)中注意分析化学式确定氧元素质量分数,注意对基础知识的理解掌握.



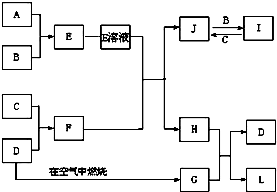
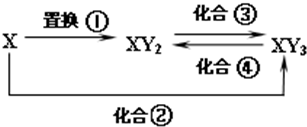 元素X的单质、Y单质及X与Y形成的化合物能按如下图所示的关系发生转化,图中化合反应均为与X或Y单质的反应,且Y单质为气体,
元素X的单质、Y单质及X与Y形成的化合物能按如下图所示的关系发生转化,图中化合反应均为与X或Y单质的反应,且Y单质为气体,